三维模型揭示了细胞微环境与癌症干细胞之间的协同作用

由于a *STAR的研究人员,对抗恶性胶质瘤等致命脑癌的斗争可能很快就会从一项重大突破中受益。研究小组发现了癌细胞生长与其微环境之间的新联系。
阀杆细胞肿瘤推动了某些癌症的发展和耐药性,包括脑癌,这阻碍了抗癌治疗。它们的干细胞性,即生长、自我更新和分化成各种癌细胞的能力,受其微环境的影响。这解释了与其他细胞、粘附分子和细胞周围的基质的相互作用,也称为细胞外基质。
除了作为细胞的支持,细胞外基质介导细胞信号转导,并在促进癌细胞干细胞性中不可或缺。然而,研究集中在细胞内的信号通路来评估癌症的干细胞性,因此对微环境的作用知之甚少。
为了阐明细胞外基质对癌症干细胞的贡献,来自a *STAR生物工程与纳米技术研究所的Andrew Wan领导的团队使用了一种涉及脑癌三维模型的方法。在这个模型中,缠结的静电纺丝聚苯乙烯纤维为细胞培养提供了多孔支架。纤维上涂有特异性涂层细胞外基质蛋白层粘连蛋白。
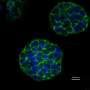
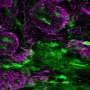
研究人员在3D模型和二维传统聚苯乙烯组织培养板中培养了取自恶性脑肿瘤胶质母细胞瘤的细胞,并监测了它们的生长情况(见图)。基因和蛋白质表达研究表明,3D培养系统比2D培养系统在更大程度上提高了肿瘤的干性。
Wan的团队进一步发现,3D系统和细胞外基质共同促进干细胞生长。具体来说,他们发现有证据表明,胶质母细胞瘤细胞膜中的两种整合素——蛋白质——通过与层粘连蛋白相互作用促进了癌症干细胞样细胞的形成。
美国国家神经科学研究所的同事们通过计算方法分析患者神经胶质瘤数据库,证实了这些观察结果。“我们的合作者表明,这些相同的蛋白质通常在更多积极的脑部肿瘤”,Wan说。
Wan解释说,这些发现为未来的抗癌治疗方法提供了一个新的视角。“我们对实验结果感到兴奋,因为我们在开始实验时没有预料到如此显著的效果,”他说。
Wan的团队目前正在研究相互作用的过程脑癌细胞和细胞外基质在3D培养系统中产生干性。他补充说:“了解这是如何发生的,也许有一天会有助于解决胶质母细胞瘤的问题。”
进一步探索











用户评论