新的见解β淀粉样蛋白在阿尔茨海默病中的作用

新阿尔茨海默病研究技术细节,迅速措施水平的大脑损害蛋白质片段,和深入了解为什么在一个特定的基因突变增加了患该疾病的风险。
这两项研究,从圣路易斯华盛顿大学医学院的研究人员,是网上的实验医学杂志。
新的测量技术可能会导致一个更好的了解β淀粉样蛋白与阿尔茨海默病相关,一个关键的蛋白质,产生和删除大脑,这将帮助科学家设计治疗限制蛋白质的积累。同时,遗传观点表明,大脑自身的免疫细胞包含损害是至关重要的,因为太有太多的β淀粉样蛋白。
当你使用你的大脑——计划一顿饭,记住路线到商店——你的神经元释放的分子称为β淀粉样蛋白,作为副产品的正常功能。在健康的人蛋白质片段清除之前,可以做任何损害。在阿尔茨海默氏症患者,清除受损,和β淀粉样蛋白构建成块称为斑块。
许多研究了阿尔茨海默氏症的治疗旨在减少β淀粉样蛋白在大脑中。约翰Cirrito博士,神经学副教授,卡拉Yuede,博士,神经病学的教练,和他的同事们开发了一种新的技术措施实时大脑中β淀粉样蛋白含量的变化情况。之前的技术允许只测量一次一个小时。
“过去14年来我们有技术,我们将做一些鼠标,给它一个药物,它执行一个特定行为,我们发现其淀粉样β蛋白水平怎么了一小时后,“Cirrito说,资深作者。“等待那么久只是不够好。神经活动发生在快速的时间尺度,我们需要看到干预之间的直接联系和β淀粉样蛋白的水平。”
在人群中,β淀粉样蛋白释放电子当暴露于少量的电压。这些电子可以测量电流,电流成正比的β淀粉样蛋白的量。
专门研究人员连接抗体,检测β淀粉样蛋白在一个很小的电极,电击和少量的电压测量产生的电流。
“人们已经使用这种方法对其他分子,但探测器显微镜幻灯片的大小,“Cirrito说。“我们改编成五微米纤维,比人的头发细,所以它可以植入大脑。”
因为鼠标β淀粉样蛋白,与人类的版本,不产生电流接触电压时,研究人员利用转基因小鼠产生人类β淀粉样蛋白。他们把老鼠药,阻止新的β淀粉样蛋白的生产,和监控现有的β淀粉样蛋白的速度消失。
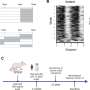
实验发现奇怪的东西:一个间隙通道迅速清除β淀粉样蛋白在较高的水平,但不同,慢一个后来成为占主导地位的水平下降。这些结果与研究Cirrito自己等,曾发表,建议间隙率和相对重要性不同的途径不依赖于β淀粉样蛋白的浓度。
“这是很重要的,如果你设计一个治疗策略对阿尔茨海默氏症,”Cirrito说。“如果你遇到第一个途径,你可能有一个效果很快,但是你可能无法降低淀粉样蛋白β水平超过了某一程度。你不得不考虑针对多个通路。”
突变增加风险
在另一项研究中,另一个华盛顿大学的研究小组发现,在一个特定的基因突变增加阿尔茨海默氏症的风险通过影响细胞的功能分子碎片清理。
人携带基因的突变形式TREM2已经增加了五倍患老年痴呆症的风险。基因编码的一种蛋白质,在大脑中,发现只有一个类型被称为小神经胶质细胞的免疫细胞。
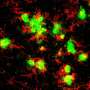
“我们发现,小胶质细胞没有TREM2异常表现,”文章的第二作者说马可报摊,医学博士,医学博士,教授罗伯特·摇滚Belliveau病理学。“我们推测,在老年痴呆症患者,随着时间的推移,小胶质细胞不含有β淀粉样蛋白的积累,导致增加他们的大脑受损。”
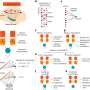
小胶质细胞是大脑的保洁人员打扫,席卷和摧毁死亡细胞,微生物和分子碎片,包括β淀粉样蛋白。当TREM2检测到一种脂肪的存在称为磷脂,它发送一个信号,激活小胶质细胞。
找出为什么失去TREM2函数提出了阿尔茨海默氏症的风险,报摊,文章的第二作者David Holtzman医学博士和他的同事们淘汰TREM2基因在小鼠体内有遗传倾向发展淀粉样斑块。
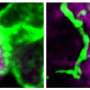
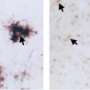
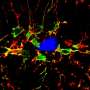
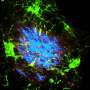
与TREM2老鼠的大脑中,小胶质细胞包围中的淀粉样蛋白斑块,但在那些没有TREM2,小胶质细胞分散。没有小胶质细胞包围了他们,斑块分布和标记神经元损伤的上升,虽然β淀粉样蛋白的总量保持不变。
“如果你没有TREM2,斑块扩散到大脑和破坏的关键部分神经元,“报摊说。
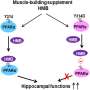
识别阿尔茨海默氏症的小胶质细胞的作用对治疗手段的发展开辟了可能性。TREM2分子通路的第一步,从检测磷脂激活细胞。小胶质细胞也熊抑制性受体表面,发送信号通过一个并行分子通路,以防止细胞被激活。
“你可以目标不仅TREM2 TREM2通路中的任何分子使小胶质细胞更活跃,“报摊说。”或者你可以阻止任何一步抑制途径。”
另一种可能性是抗体作为斑块之间的桥梁,一边小胶质细胞。在阿尔茨海默氏症患者小神经胶质细胞自己不环绕斑块,如那些TREM2缺陷或另一个分子通路,抗体可以使细胞斑块。
更多信息:卡拉·m·Yuede et al .体内快速测量β-amyloid揭示两相的间隙动力学阿尔茨海默病小鼠模型,《实验医学杂志》上(2016)。DOI: 10.1084 / jem.20151428