代谢物的多发性硬化症药物可以安全、有效治疗帕金森病

药物的代谢物是帮助病人战斗多发性硬化症似乎明显减缓帕金森病的发作,研究人员说。
口服药物,dimethylfumarate或DMF,及其代谢物,monomethylfumarate,或MMF, Nrf2活性增加,蛋白质,帮助保护身体氧化应激和炎症,这两种疾病的标志,博比·托马斯博士说,神经科学家的药理学和毒理学在乔治亚州奥古斯塔大学医学院的。
但是新的研究提供了第一个证据,代谢物,也就是父的活跃部分药物,Nrf2更直接的目标,可能减少已知父药物的副作用,包括冲洗、腹泻、恶心、呕吐、腹部疼痛和大脑感染脑病,Thomas说,该研究的通讯作者《神经科学杂志》上。
尤其是胃肠道副作用会加剧一些问题病人帕金森病已经经历,约翰·摩根博士说,神经病学家、神经学家和帕金森病MCG的神经学专家。除了破坏神经元在大脑中产生多巴胺,一种神经递质,使运动和学习,帕金森氏症引起胃肠道神经细胞死亡和严重的便秘等相关问题。
“Nrf2是我们对氧化应激保护机制,”托马斯说。多发性硬化症和帕金森的共同点的证据Nrf2活性的下降路径产生了兴趣帕金森症等神经退行性疾病的药物。
DMF被批准多发性硬化症三年前由美国食品和药物管理局。而其代谢物MMF并不像父母那样强大的药物在增加Nrf2活动,这项新研究表明,其作用就足以显著减缓损失以及父母产生多巴胺的神经细胞的药物,在帕金森病的动物模型。
在他们的模型中,老鼠注射了神经毒素MPTP药物经验显著损失,产生多巴胺的神经细胞失去一半在少数天,快速开发它们帕金森症状。病人,另一方面,多年来慢慢出现症状。他们寻求医疗护理,病人可能已经失去了30 - 50百分比的多巴胺能神经元,摩根说研究合著者。“演讲后疾病的。”
适应的压缩时间在他们的模型中,几个每日剂量药物开始工作之前,需要研究人员首先给小鼠注射药物或代谢物的前一天他们开始毒素。
位于darker-pigmented中央产生多巴胺的神经细胞部分大脑的称为黑质。即使在没有疾病,使得这些神经元多巴胺是一个充满压力的工作使得他们更脆弱,实际上导致氧化应激在健康的情况下,摩根说。做一个困难的局面更糟糕的是,增加氧化应激可以使多巴胺神经元毒性,他说。
增加Nrf2活性,父药物DMF似乎也第一次让坏事情变得更糟。DMF增加氧化应激通过消耗天然抗氧化剂,谷胱甘肽,并减少细胞强国的力量,被称为线粒体,通过限制他们使用氧气和葡萄糖的能力让能源中产生多巴胺的细胞的生存能力,托马斯说。
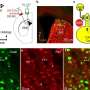
代谢物MMF似乎更直接激活Nrf2,实际上增加了谷胱甘肽和改善线粒体功能,大脑细胞研究显示。虽然父母药物最终产生更高的Nrf2激活,研究人员发现MMF效应足以阻止戏剧性的神经元损失在动物模型。
DMF和MMF放缓神经元损失更正常的水平,继续制造多巴胺的神经元幸存下来。炎症和氧化应激水平也显著降低,研究人员说。
下一步,他们正在向一个临床试验的MMF患者早期帕金森病。虽然人类代谢物可以很容易地制定,它尚未完成,托马斯说。
“如果我们能赶上他们足够早,也许我们可以减缓疾病,”摩根说。“如果它可以帮助给5至8年的生活质量改善的那将是伟大的为我们的病人。”
临床研究帕金森病的药物正在计划在英国和其他代谢物的类似物,可用于临床,研究人员认为这最终将患者的最佳选择,正在开发中。
氧化应激是机体的副产品利用氧气。氧自由基,生成的使用,是不稳定的分子,可以干扰正常细胞功能,被认为有助于各种条件与通常的衰老阿尔茨海默氏症。给抗氧化剂,例如维生素E,工作更像拾荒者围巾自由基,并没有在防治神经退行性疾病,托马斯说。他的乐观,直接针对Nrf2至少将有效地减缓疾病,但仍然是一个需要临床安全Nrf2活化剂。
Nrf2通路活性随着年龄的增长会慢慢下降。锻炼上调Nrf2,和摩根经常鼓励病人尽可能活跃。一小群帕金森患者在欧洲有一个集中的激活Nrf2至少延迟他们的疾病发作。帕金森病往往是诊断定在50年代和60年代早期,男性更常见。
一个关注长期提升抗氧化和抗炎药物分子DMF和MMF是创建一些同样的问题,给器官移植患者免疫抑制药物。慢性免疫反应的抑制使患者更容易受到侵略者像癌症和感染。
帕金森病基金会估计有七个与帕金森全世界1000万人的生活。