癌细胞筛查的突破推进了儿童白血病的个性化治疗
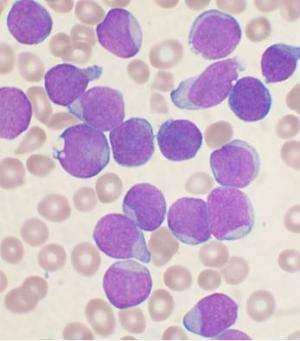
纽卡斯尔大学的研究人员已经能够准确地预测白血病治疗后癌症复发的儿童对进一步治疗的反应。
这一发现是同类研究中规模最大的,它将使医生能够分析癌细胞的遗传特征,从而进行个性化治疗和改善存活率.
由于研究,被诊断患有急性淋巴细胞白血病(儿童癌症中最常见的一种)的儿童中,有多达90%将获得长期治愈。然而,对于那些疾病复发的儿童,预后要差得多,只有不到六成的儿童存活超过5年。
发育中的遗传断层白细胞启动并推动白血病的增长。已知遗传错误的类型和组合会影响儿童是否可能对初始治疗反应良好,进而影响他们的生存机会是好还是坏。基因筛查已经被用于在诊断时量身定制治疗,确保儿童接受最合适强度的化疗。到目前为止,人们还不太清楚如果白血病复发,如何使用这些“遗传标记”来指导治疗。
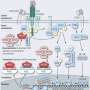
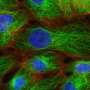
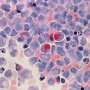
纽卡斯尔大学的科学家们在血癌慈善机构Bloodwise的资助下,分析了427名因复发而接受治疗的儿童的白血病细胞急性淋巴细胞白血病在2003年到2013年间。他们使用了包括荧光原位杂交(FISH)在内的各种基因测试,其中发光标记与DNA序列结合癌症细胞科学家可以在显微镜下观察特定的基因变化。
目前,复发性白血病儿童的分组是根据他们是否处于不良结果的标准或高风险,基于诸如儿童缓解的时间以及复发时骨髓中是否存在白血病细胞等因素。根据这些标准,目前被认为是高风险的患者将经历一场艰苦的治疗干细胞移植而标准风险患者通常会接受进一步化疗。
到目前为止,白血病患者在治疗结束后很长一段时间内复发,被认为有很大的生存机会。这些患者接受的化疗强度通常低于那些被认为风险较高的患者。由纽卡斯尔大学北方癌症研究所的安东尼·穆尔曼教授和朱莉·欧文博士领导的研究小组发现,在复发时,患有一种或多种“高风险”基因异常的标准风险组儿童对化疗反应不佳。
此外,研究人员还发现了一些基因的异常(例如TP53、NR3C1、BTG1和NRAS),这不仅提供了关于这些儿童如何以及为什么对当前治疗反应不良的额外信息,而且还为未来有类似基因缺陷的儿童如何更有效地治疗提供了有用的见解。例如,有RAS基因缺陷的儿童可能受益于一种名为“MEK抑制剂”的新药,这种药物可以特异性地杀死有RAS基因缺陷的细胞。
这项研究发表在著名杂志上血.
遗传流行病学教授Anthony Moorman是纽卡斯尔大学白血病研究细胞遗传学小组的联合领导,他说:“目前用于指导复发性白血病治疗的方法不够准确,一些被认为有很大机会存活的儿童实际上对化疗反应非常差。”在复发时筛查影响结果的关键基因异常将确保治疗可以个性化,从而提高他们的生存机会。”
研究人员还发现了一大批“低风险”儿童,遗传缺陷.当这些孩子也有良好的临床危险因素时——比如第一次缓解时间很长——他们对标准化疗的反应非常好,他们可以免于干细胞移植。
Bloodwise的研究总监阿拉斯代尔·兰金博士说:“展望孩子们复发的人通常情况较差,因此迫切需要更有效的治疗方法。这些发现代表着对这些患者的个性化治疗的发展向前迈出了重要一步。需要进一步的研究来测试裁剪是否治疗基于遗传因素的复发性疾病确实提高了生存率。”
进一步探索