microRNA在重大抑郁症中起作用

一个微小的RNA似乎在产生重大抑郁症中起作用,这种精神障碍每年在全球影响多达2.5亿人。
重度抑郁症,正式称为严重抑郁症或MDD,会带来自杀的风险增加,据报道导致低背痛后的第二年残疾。
伯明翰大学研究人员的阿拉巴马大学发现,在实验大鼠的大脑中,这种microRNA的数量显着升高,在诊断为MDD和MDD患者的周围血清中,死亡的人类死亡后脑中会导致皮质酮治疗引起的抑郁症。根据Yogesh Dwivedi博士领导的一项研究,Elesabeth Ridgely Shook exhok又赋予了精神病学系UAB情绪障碍计划转化研究教授兼转化研究主任。
因此,这种microRNA(mir-124-3p)是新型药物发育的潜在治疗靶标,它可以作为MDD发病机理的推定生物标志物。
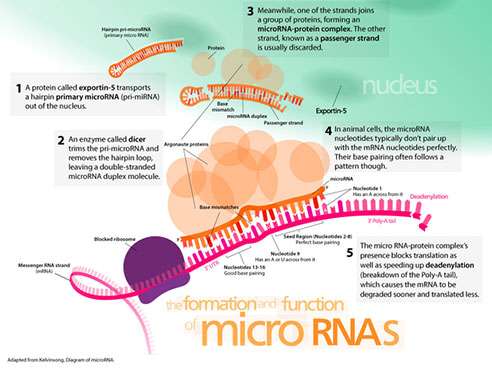
微RNA或miRNA与MERNA从细胞核导出并由酶团队处理后与信使RNA相互作用。miRNA是细胞中基因调节的强大参与者,大脑中有1300多个不同的miRNA。
在以前的工作中,德威维迪及其同事们看到一组miRNA在该公司中进行了协调监管前额叶皮层MDD受试者的大脑。以控制大脑的执行功能而闻名的前额叶皮层通过调节称为下丘脑 - 垂体 - 肾上腺肾上腺轴的内分泌腺而与应力反应有关。肾上腺在人类和啮齿动物的皮质酮中产生应力激素皮质醇。
为了了解压力是否在前额叶皮层miRNA的协调调节中起作用,UAB研究人员随后转向大鼠抑郁模型。他们发现,用皮质酮治疗以诱导抑郁症行为的大鼠显示前额叶皮层中miRNA的协调失调,最显着影响的miRNA是miR-124-3p。
他们当前的论文,在期刊上预览神经心理药理学,检查了miR-124-3p在MDD发病机理中的相关性。
研究人员使用基因组序列的计算机分析:
- 确定了八个高潜力靶基因为了通过miR-124-3p结合,据报道其功能在压力和MDD发病机理期间的功能也至关重要。这些潜在靶基因中的四个在皮质酮处理的大鼠的前额叶皮质中显着下调,并且该下调与miR-124-3p水平呈崩溃。
- 表明,显着下调的四个基因具有在广泛较高脊椎动物物种的进化中保守的miR-124-3p结合位点。
在培养中生长的神经母细胞瘤细胞中:
- miR-124-3p的过表达导致两个潜在靶基因的显着下调。
在用皮质酮治疗的抑郁症大鼠的前额叶皮层神经元中:
- 通过免疫沉淀的RNA诱导的沉默复合物测量,miR-124-3p与两个潜在靶基因的显着结合被观察到了两个潜在的靶基因。
- 成熟的miR-124-3p的基因座特异性起源在3号染色体的位点,三个可能的染色体位点中的位点,两个CpG“岛”,可以通过DNA甲基化在表观遗传修饰的位点鉴定出DNA甲基化的位点。MiR-124染色体上的基因启动子。
- 发现该miR-124-3启动子在皮质酮治疗的大鼠中是甲基化的,并且一个DNA甲基转移酶-DNMT3A的基因表达受到了显着抑制。
对于人类:
- 在15个对照和15个MDD受试者的验尸后大脑中,MDD组的miR-124-3p表达显着增加,并且三个潜在靶基因的表达显着降低。
- 与17例健康对照相比,在18种抗抑郁药的MDD患者的血清中,miR-124-3p的水平明显更高。
UAB研究人员总结说:“总共是“这是维特罗和体内水平上的首次全面和机械研究,这表明,不仅在整个miR-12p表达中都存在一致的抑郁症相关变化不同的物种,但也是该miRNA的靶标的基因,高度失调,在功能水平上显示出改变的反应。”