基因组的非编码部分被发现在癌症中起作用
人体产生100,000个或更多不同的蛋白质。然而,令人惊讶的是,只有两种人类基因组实际编码蛋白质。其余的基因组的近80%转录成没有蛋白质代码的RNA。科学家面临的两个大问题是:这个“非编码”RNA实际上是多少?它是否在疾病中发挥作用?
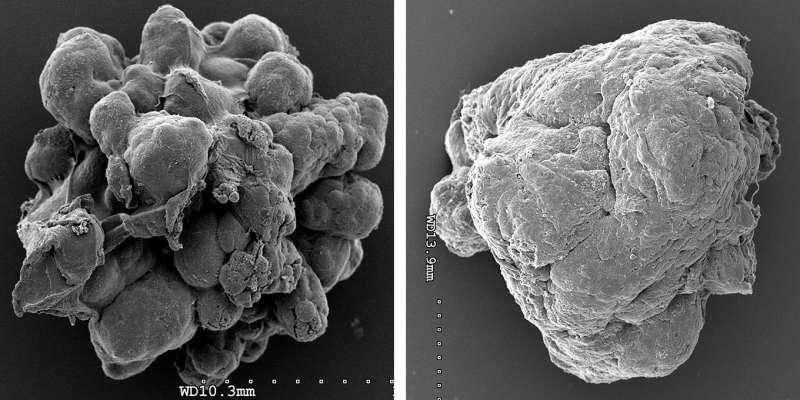
冷泉港实验室(CSHL)的科学家团队筛选了数千个非编码的RNA,以发现那些在两种类型的侵袭性乳腺癌中表达的那些。因为他们今天描述了出现在纸张中细胞的报道当它们减少了从乳腺肿瘤样本中这些RNA的一些最表达的部分的水平时,癌症扩散的细胞特征显着降低。
在为数不多的几种不同类型的非编码RNA中,数量最多、理解最少的是长链非编码RNA (lncRNAs)。大约16000个lncrna已经在人类中被识别出来,但其中绝大多数的功能尚不清楚。
“因为那么大部分基因组被转录成RNA,那么似乎就有没有真正研究过的潜在治疗性的潜在治疗目标,”团队领导者,CSHL教授David Spector说,他也是实验室研究总监。
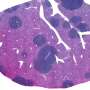
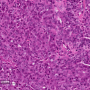
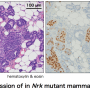
虽然大多数lncrna的确切功能仍有待发现,但已经有研究表明,在某些情况下,它们的过表达与特定癌症有关,包括乳腺癌、前列腺癌和白血病。今年早些时候,斯派特的团队证明了这一点一个lncRNA叫Malat1是乳腺癌进展的关键调节因素。在腔性B乳腺癌小鼠模型中,消除这一特殊的lncRNA会导致原发肿瘤内的细胞改变特征,并导致转移的显著减少。
“这项研究为我们寻找其他可能过表达并产生影响的lncrna提供了重要的动机乳腺癌,”斯佩克特说。
在博士后Sarah Diermeier的带领下,Spector和他的团队系统地筛选了大量的lncrna数据库,以确定那些相对于正常乳腺细胞而言,在肿瘤中表达更频繁的lncrna。
该团队发现了几百LNCRNA,其表达于它们的两种类型的侵袭性小鼠肿瘤中的正常水平,它们测试:Luminal B和Her-2阳性。然后,它们进行了广泛的计算分析,以优先考虑这些LNCRNA的30个子集中,它们被称为乳腺肿瘤相关的RNA或Matars。
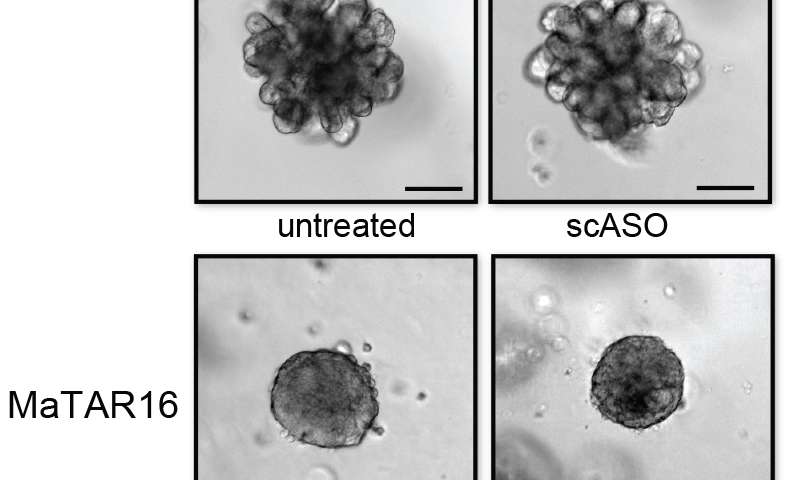
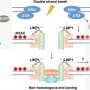
与Ionis Pharmaceuticals,Spector和Hcolleagues合作设计了一系列紧密结合的分子,从而破坏特定的RNA序列。它们使用这些所谓的“反义”分子来消除乳腺癌衍生的有机体的个体matars,肿瘤细胞的三维模型,其代表真实肿瘤的许多特征。
研究人员发现,单独去除这些类器官中30种matar中的20种会减少与癌症相关的特征,包括细胞增殖、侵袭和迁移。
“我们现在有一种创新的方法来破坏活细胞内的RNA靶标并评估肿瘤是否依赖于它们,以便存活,”Spector说。
该团队的下一步是施用反义分子,以降解小鼠的特定Matars,希望这将减少原发肿瘤质量和/或转移。如果这些实验成功,SPENTER的团队将在人肿瘤样品中进行额外的临床前测试,以更好地确定哪些患者的亚组将受益于抗义分子治疗,以消除某些LNCRNA或LNCRNA簇。
“我们认为这些测试将对个性化医学进行特殊相关性,”研究第一作者Diermeier“我们想象一种情况可以从个人的肿瘤中衍生出有机体,在一道菜中长大,并充当一个平台,以弄清楚哪个反义分子包含患者的最佳治疗。“
本释放中描述的研究得到了国家癌症学院授予5PO1CA013106-inclet 3,Manhasset妇女联盟对乳腺癌,西蒙斯基金会和癌症中心支持赠款给冷泉港实验室(2P30CA45508)。
“乳腺肿瘤相关rna影响肿瘤细胞增殖、侵袭和迁移,”2016年9月27日在线发表细胞的报道。作者是Sarah D.Idermeier,Kung-Chi Chang,Susan M.Fuerier,Junyan Song,Osama El Demerdash,亚历山大Krasnitz, Frank Rigo, C. Frank Bennet和David L. Spector。该文件可在http://www.cell.com/cell-reports/newarticles








用户评论