研究表明,肠道细菌有助于脊髓损伤的恢复
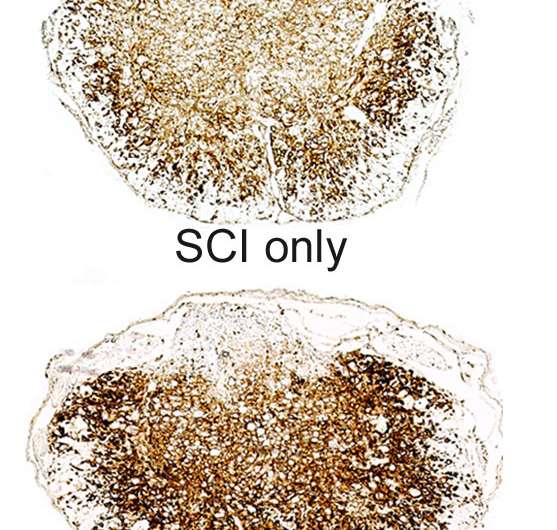
俄亥俄州立大学的研究人员发现,脊髓损伤会改变肠道中细菌的类型,这些变化会加剧神经损伤的程度,损害功能的恢复。Kristina A. Kigerl等人的研究,“肠道生态失调损害脊髓损伤后的恢复”,将于10月17日在线发表实验医学杂志的研究表明,用益生菌来抵消这些变化可以帮助患者从脊髓损伤中恢复。
生活在胃肠道中的数万亿细菌被统称为肠道细菌肠道微生物组.这种微生物群落的破坏或生态失调发生在非致病性的情况下肠道细菌被致病性炎症细菌耗尽或淹没。自身免疫性疾病(包括多发性硬化症、I型糖尿病和类风湿性关节炎)与生态失调有关,它与神经系统疾病的发生或进展有关,包括自闭症、疼痛、抑郁、焦虑和中风。
创伤性脊髓损伤有继发性影响或合并症,包括肠道失控,这可能导致生态失调。作者推断,如果肠道微生物组发生任何变化,它们可能反过来影响脊髓损伤后的恢复。
在脑和脊髓修复中心(Center for Brain and Spinal Cord Repair)的菲利普·g·波波维奇(Phillip G. Popovich)的指导下,研究人员发现脊髓损伤显著改变了小鼠的肠道微生物群,诱导肠道细菌迁移到身体的其他组织,并激活与肠道相关的促炎免疫细胞。
肠道细菌变化最大的小鼠往往从损伤中恢复得较差。事实上,当小鼠在脊髓损伤前用抗生素破坏它们的肠道微生物群时,它们表现出更高水平的脊髓炎症和降低的功能恢复。相比之下,当受伤的老鼠每天服用益生菌来恢复健康的肠道细菌水平时,它们的脊髓损伤更少,后肢活动也恢复得更多。
益生菌含有大量的乳酸菌,激活了一种肠道相关的免疫细胞调节T细胞,可以抑制炎症。这些细胞可以防止损伤后脊髓的过度损伤。此外,益生菌可能通过分泌促进神经元生长和功能的分子来促进脊髓恢复。“这两种机制中的任何一种或两种都可以解释肠道微生物群的损伤后破坏如何导致糖尿病的病理脊髓损伤以及益生菌如何阻止或逆转这些影响,”波波维奇解释道。
波波维奇继续说:“我们的数据强调了肠-中枢神经系统-免疫轴在调节脊髓损伤后恢复中以前未被认识到的作用。”“‘以脊柱为中心’的修复方法不应该再主导受影响个体的临床护理研究或标准。”
进一步探索








用户评论