线粒体控制着干细胞的命运
在慢性疾病期间肠上皮细胞发生了什么?慕尼黑技术大学营养和免疫学主席进行的基础研究(Tum)通过产生新的模型系统解决了这个问题。功能性线粒体在细胞稳态中发挥着决定性的作用,但是在线粒体中的抗应力计划的重要球员被关闭时会发生什么?一方面,这导致干细胞的损失,但另一方面导致干细胞的损失,它落入运动中的愈合过程。
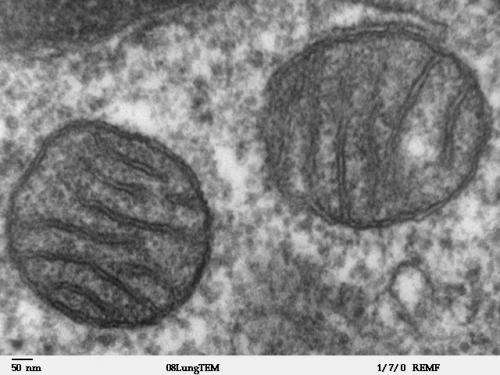
人的肠道系统面积约300 - 500平方米,因为它有许多突出(绒毛)。充满小肿块的肠壁每4到5天就会完全更新一次,这是一个有指导的过程干细胞。线粒体是细胞的强者,并通过呼吸提供能量,并在这一过程中发挥关键部分。
当肠上皮细胞的自我更新被打断时,例如由于有缺陷的线粒体,慢性炎症可能在极端条件下产生。“我们谈到了细胞压力,”慕尼黑技术大学营养和免疫学和食品健康研究所执行董事(Ziel)举行的德克大厅教授(Tum)。如果发生细胞应力,则将其放在图形上 - 使助手被激活,以确保涉及更新过程中的蛋白质在细胞中适当地折叠,以便保持稳态肠粘膜。热休克蛋白(Heat shock protein, HSP) 60就是其中的一种调节因子,它对维持线粒体的状态至关重要肠上皮细胞。
失活热休克蛋白的研究
在一项刚刚发表的研究中自然通讯Haller和他的团队对这种蛋白HSP60进行了更仔细的检测。它与科学家们所称的未折叠蛋白反应(UPR)密切相关——可以理解为细胞抗应激程序的一个组成部分。当这个关键的调节因子HSP60在肠道中失活时,会发生什么?线粒体缺失时,细胞内如何反应?
一方面,减少了呼吸能力和细胞ATP水平,这两个关键任务都是线粒体的关键任务,细胞的强者。与此同时,Haller教授和他的团队观察到没有HSP60的所有细胞都提出了变化。干细胞丧失了它们的自我再生能力,同时周围上皮细胞开始增长计划。
由于生长环境的诱导,组织再生
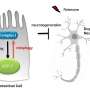
“但对HSP60缺乏的反应是令人震惊的”,因为虽然干细胞失去了它们的特征性质,但周围肠道壁壁中的应力细胞激活了首先在组织再生中最终结转的增长方案。“具有破坏线粒体功能的细胞将生长因素作为“帮助”发送出来。使用应力响应计划,他们确保与完整的线粒体居中的居住干细胞大量分裂;这些新的完整细胞然后替换另一个压力的细胞。
因此,缺乏HSP60导致了细胞间的通信建立,触发了一种之前未知的愈合机制,这可能在肠损伤或炎症后具有重要意义。“这表明了线粒体在调节肠道组织更新方面的基本作用,以及它们如何可能导致慢性肠道疾病,”Haller说。因此,当肠道处于永久的炎症或应激状态时,干细胞就会永久地过度刺激自我更新,这可能会促进肿瘤的发展。
进一步探索












用户评论