损坏蝾螈再生中鉴定为关键蛋白质的作用

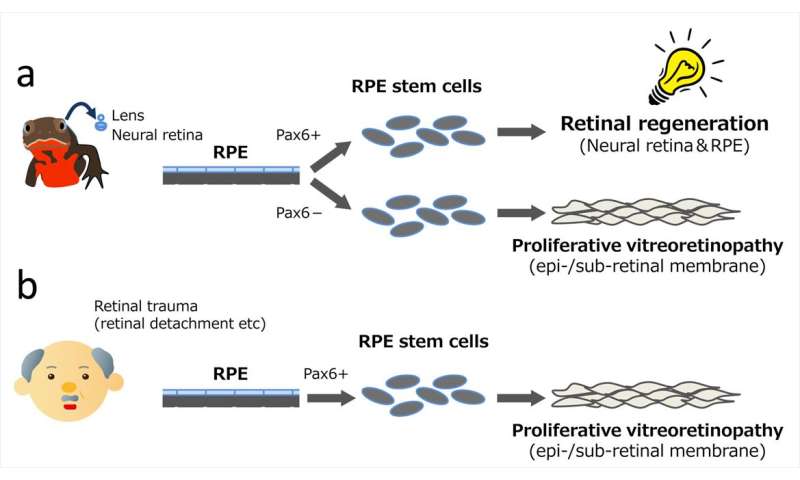
在成年脊椎动物的视网膜后部有一层高度分化的细胞,称为视网膜色素上皮(RPE)。这些细胞在成年人身上通常不会增殖或迁移,但在人类身上,它们会在视网膜损伤时增殖或迁移。然后,它们会经过一个多能性的过渡状态,有可能变成不止一种细胞类型,最终转化为可以愈合伤口的细胞,但最终会导致失明。这会导致视网膜疾病,如增殖性玻璃体视网膜病(PVR)。
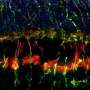
在成年蝾螈身上,也可以看到类似的过程,但有一个关键的不同之处:它导致了功能完整的视网膜和RPE的再生,即使视网膜已经通过手术从眼睛中移除。蝾螈的这种再生过程的机制仍然是一个谜,但是日本筑波大学领导的研究人员通过创造一种在RPE干细胞中缺乏Pax6蛋白表达的转基因蝾螈,已经阐明了这一课题。在这种类型的蝾螈中,视网膜再生被抑制,RPE干细胞取代了从创伤中恢复的人类RPE细胞。
这项研究发表在科学报告。
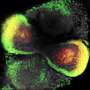
PAX6在胚胎发育期间控制组织和器官的形成,并在出生后调节眼睛的部分中的基因表达。以前发现它以经历重编程的RPE细胞重新表达。在这种新研究中,PAX6基因的沉默导致RPE细胞在除去后的rPE细胞行为的异常。细胞能够繁殖和迁移,但不能形成新视网膜或更新RPE。“我们观察了缺乏PAX6表达的RPE细胞中的蛋白质,蛋白质,平滑肌肌动蛋白等蛋白质的表达,”第一作者Martin Miguel Casco-Robles说。“这些细胞形成了类似于形成PVR中伤口的膜的结构组。”
Pax6基因的敲除表明了Pax6基因在决定RPE细胞的视网膜再生或获得膜性表型方面的重要性。通讯作者Chikafumi Chiba说:“蝾螈再生过程的进化很可能是在现有的导致视网膜疾病的机制(如PVR)发生改变之后发生的。”“如果我们能学会控制这种机制,它可能为视网膜问题提供一种新的治疗方法,能够让受影响的患者再生视网膜。”
进一步探索







用户评论