研究表明神经生长蛋白控制血糖
由约翰·霍普金斯大学(John Hopkins)大学生物学家领导的研究表明,生化途径的起作用有助于控制血液中的葡萄糖,这一发展可能会导致糖尿病治疗。
在本期发表的论文中发育细胞,杰西卡·霍兹(Jessica Houtz)是约翰·霍普金斯(Johns Hopkins)生物学系的Rejji kuruvilla的研究生,表明调节神经细胞发育的蛋白质也在促使胰腺中的细胞释放胰岛素的细胞中起作用保持正常水平血糖。
库鲁维拉(Kuruvilla)与主要作家约翰·霍普金斯(Johns Hopkins)的同事霍兹(Johns Hopkins Houtz)和生物学系的博士生菲利普·博登(Philip Borden)和亚历克西斯·科斯林(Alexis Ceasrine)合作。牛津大学药理学系的Liliana Minichiello也参与其中。
这项研究可能与2型糖尿病有关,这是该疾病的最常见形式,影响了近十分之一的美国人。这种形式的疾病可以在生命的任何时候出现,人体会产生胰岛素,但要么不足以释放,要么没有有效地使用调节化学物质来控制血糖。在童年时期出现的1型糖尿病中,免疫反应消失了,破坏了人体完全产生胰岛素的能力。
胰岛素的研究代表了库鲁维拉的绕道,其工作重点是周围神经系统的发展。她研究了一组称为神经营养蛋白的蛋白质,特别是神经生长因子[NGF]。这些蛋白质培养神经元的生长,即神经系统的细胞。
一段时间以来,神经元和胰腺β细胞,或β细胞位于称为Langerhans胰岛胰岛并产生胰岛素的簇中,在分子构成和信号受体中具有许多相似之处。受体是对特定化学物质反应并在生化途径中起关键作用的细胞表面上的蛋白质。神经元和胰腺β细胞都有神经营养蛋白的受体。
库鲁维拉说:“看到NGF受体中存在于β细胞中,这一项目是激发的。”她说的是:“这些受体在外面做什么神经系统?”
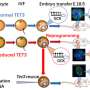
事实证明,NGF在成熟的胰腺中执行功能,这与支持神经元无关。具体而言,研究团队追踪了一系列的生化信号,表明血糖升高会导致NGF从胰腺中的血管中释放出来,然后NGF信号会促使胰腺β细胞放松其刚性的细胞骨骼结构,从血液。尽管β细胞也使NGF成为NGF,但Kuruvilla和她的团队发现,胰岛素分泌所需的是从血管中释放出来的NGF。
在小鼠和药物中使用遗传操纵来阻断β细胞中的NGF信号传导,它们能够破坏该信号传导序列的不同元素,以表明这种经典的神经元途径是增强小鼠中胰岛素分泌和葡萄糖耐受性的必要条件。重要的是,Kuruvilla及其同事发现NGF的增强能力胰岛素分泌响应于高葡萄糖也发生在人β细胞中。
目前尚不清楚该系统如何影响糖尿病患者。库鲁维拉说:“我们非常有兴趣知道糖尿病前个体是否会破坏这一途径的各个方面。”确定结合和激活胰腺中NGF受体的NGF或小分子是否可能在治疗2型糖尿病的治疗中可能使用。这些是在进一步研究中要提出的问题。