鉴定为靶向胶质瘤脑肿瘤的有吸引力的药物候选者
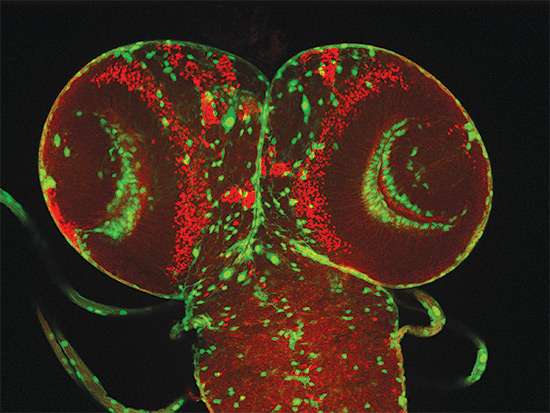
在今天发表的论文中癌症研究,研究人员:1)鉴定与腐蚀性胶质瘤脑肿瘤相关的生物标志物酶,2)揭示该酶的调节机制,3)用胶质瘤的小鼠模型表现出胶质瘤的小鼠模型,用于它们已经开发的小分子抑制剂。
抑制剂Ga11保持核心结构,其类似于生物标志物酶的天然抑制剂;但抑制剂已被修改以帮助它通过血液 -脑障碍。
“原则上,这两种特征都使GA11成为一种有吸引力的药物候选物,以靶向胶质母细胞瘤多形肿瘤中的胶质瘤干细胞,”ICHIRO NAKANO,M.D.,PH.D.及其同事。
伯明翰大学阿拉巴马大学神经外科和学术神经外科教授Nakano以及意大利比萨大学的Vito Coviello和Concettina La Motta Concettina La Motta,正在进行GA11及其类似物的临床前评价。
胶质母细胞瘤多形形或GBM,是一种强大的癌症敌人。纳卡诺说,过去30年来,只有两种治疗性改善,增加了五个月到15或16个月的患者的平均存活。
GBM肿瘤是不同细胞的混合,其与疗法不同。少量的胶质瘤干燥的细胞或GSCs,驱动GBM的肿瘤性,因此是可能治疗的主要靶标。一种称为间充质GSC的GSC亚型更加恶性和最多的治疗,因此纳卡诺和研究人员推出了鉴定在间充质GSC中活性的调节分子可能导致新颖和有效的治疗剂。
研究细节
Nakano和同事发现一种形式的酶醛脱氢酶-Aldh1a3-是间充质GSC的特定标志物,他的基团是第一个表明,在GBM肿瘤中,具有高水平Aldh1a3的细胞的细胞的异质混合物中。表达比Ald1A3中低的细胞更含致瘤瘤。
研究人员还发现FoxD1转录因子调节间充质GSC中的Aldh1a3的产生。在来自患者的高等胶质瘤的临床样本中,FoxD1和Aldh1a3的表达水平与疾病进展 - 胶质瘤与高水平的疾病进展 - 龋齿与低水平的胶质瘤更快地致死。
令人惊讶的是,驱动人类中间充质GSC致瘤性的相同机制在进化的遥远的生物中起作用,果蝇。研究人员发现,敲击Aldh1a3的果蝇或果蝇版的果蝇或果蝇版的表达或果蝇版的果蝇版植物癌模型中的脑癌模型。因此,这种信令在进化中得到了高度保守。
Foxd1转录因子在从受精卵和胚胎到胎儿的发展过程中通常是活性的,并且出生后它是沉默的。Foxd1在GBM,Nakano及其同事所说的作用表明,间充质GSCs劫持了正常胚胎发育的分子机制,以促进肿瘤生长。
在临床前测试中,GA11验证了几种方式。研究人员表明,它抑制了酵母中的ALDH,降低了间充质GSC的细胞培养球中的AldH1活性,抑制细胞培养中的胶质瘤球体的增殖,并抑制了小鼠脑中GBM的异种移植生长。
“总之,”纳卡诺和同胞研究人员写道,“Foxd1-Aldh1a3轴对于间充质GSC的肿瘤起始至关重要,从而为治疗GBM和其他Aldh1激活癌症提供可能的新分子靶标。”
Nakano表示,他对GSCS在GBM中的作用的研究只是一种治疗胶质瘤肿瘤的一种方法。其他实验室正在追求免疫疗法,使用检查点抑制剂,疫苗接种和努力来增加对放射治疗的敏感性。
Nakano说,它将服用治疗胶质母细胞瘤的组合疗法。“我们不相信一个治疗将有效。”
Nakano预计2017年推出了新的胶质母细胞瘤的新临床试验,与UAB的神经内科教授一起结合Burt Nabors,M.D。Nakano说Uab将成为这种独特试验的唯一一个针对胶质瘤干细胞的分子靶标的唯一试验的网站,该靶标与癌症研究论文中描述的目标不同。与纳卡诺的服务的推荐联系将是Lydia P. Harrell。
Nakano实验室还在脑转移,肿瘤从身体的其他部位传播到大脑中。如同高级胶质瘤源自大脑,这些转移性脑肿瘤是致命的,治疗性选项很少。Nakano认为核心干细胞基因和信号通路在胶质瘤和脑转移之间共用。
“如果是这样,”他说,“对于胶质瘤鉴定的分子靶标很可能在脑转移中必需。正在进行研究,类似于胶质瘤治疗发展,我正在努力为脑转移进行临床试验,以及医疗肿瘤学家Mansoor Saleh, M.D., Andres Forero, M.D., and others at UAB."
进一步探索













用户评论