天然存在的癌症耐药机制本身可以是治疗靶标
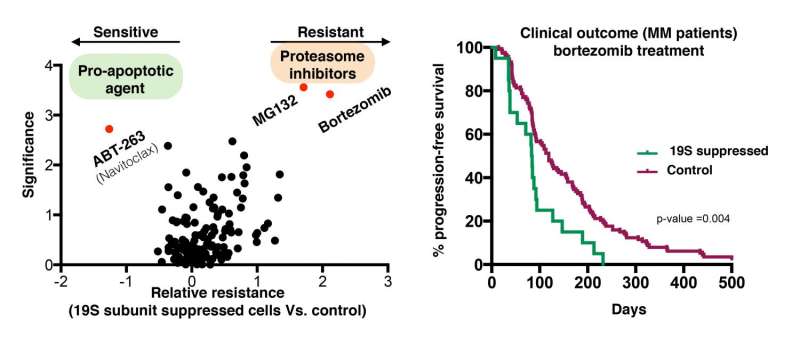
使用蛋白酶体抑制剂治疗癌症的癌症受到癌细胞产生对这些药物抗性的能力极大的限制。但白头研究所研究人员发现了这种抵抗力的机制 - 一种自然发生在许多不同的癌症类型中的机制,并且可能将脆弱性暴露于刺激天然细胞死亡过程的药物。
该发现 - 也识别可用于获得对蛋白酶体抑制性抗性状态的更深入了解的生物标志物 - 在此处报道国家科学院的诉讼程序(pnas.)在有权的文章中,抑制19s的蛋白酶体亚基标志着不同癌症中改变细胞状态的出现。
蛋白质是大蛋白质复合物,其介导蛋白质降解并在维持细胞内的蛋白质平衡方面发挥至关重要的作用。当细胞变成癌性时,巨大的应力被放置在负责维持蛋白质平衡的细胞机制上 - 并且该机器是抗癌药物的靶标蛋白酶体抑制剂。虽然蛋白酶体抑制剂在选择性杀死菜中生长的癌症肿瘤细胞(体外)的选择性杀死中非常有效,但它们在临床中的成功主要受到开发的破坏抵抗性- 它的机制知之甚少。
“然而,最近,我们发现了一种违反直觉机制,通过该反向机制可以在体外获得对蛋白酶体抑制剂的抗性,”彼得Tsvetkov解释说明pnas.文章和白头研究所的博士后研究员。“现在,在本报告中,我们表明这种机制在许多人类癌症中都在工作。此外,我们已经确定了该机制是细胞中具有广泛改变状态的症状,具有独特的基因签名可以针对现有药物的新暴露的漏洞。“特别是,该机制明显与血癌骨髓瘤患者的差异有关,其中蛋白酶体抑制剂是治疗的主干。
研究人员发现来自数千条癌症线和肿瘤的数据,发现通过抑制一种或多种细胞的蛋白酶帽亚基(这是较大的蛋白酶体的亚群)的表达,标记了对蛋白酶体抑制剂药物的抗性的那些。抑制甚至构成盖子的许多亚基的表达将损害整个帽的组装,导致蛋白酶体抑制剂抗性状态。“这一事实加强了对化疗抵抗机制的复杂性可以是多么复杂,”PNAS纸和白头研究所的高级科学家的高级作者卢克怀特林说
然而,这份新报告揭示了解决可能具有广泛效用的这种抵抗力的策略。研究人员发现,除了赋予蛋白酶体抑制剂的耐药性之外,抑制蛋白酶体亚基的表达反映了细胞基因签名的广泛重塑。此外,这也可以作为生物标志物来分层患者治疗。“签名标志着各种癌症的遗传和治疗相关的状态 - 一个可能暴露于已经在诊所已经使用的特定药物的脆弱性,”Tsvetkov观察。“癌症可以通过多种机制,遗传或表观遗传来达到这种阻力。但这些发现将我们指出,可以发展成为一种新的策略和新化合物,这些化合物可以发展为癌症类型阵列更有效,因为它们易于出现的易感性抵抗。“
进一步探索












用户评论