宾夕法尼亚大学研究人员帮助解开谜团胰腺癌的阻力标准疗法
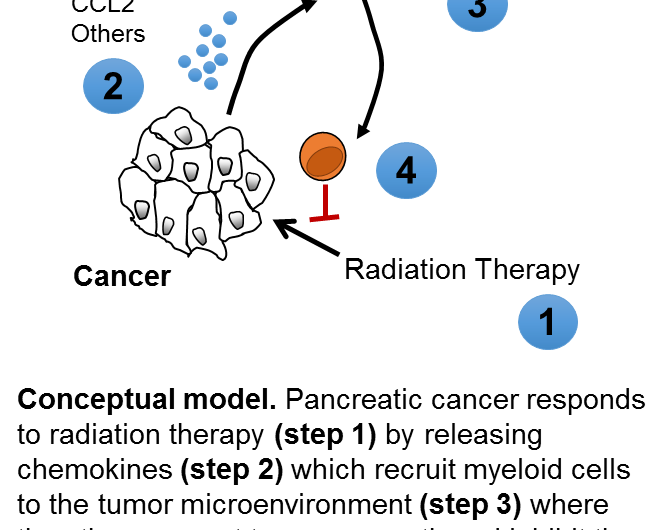
胰腺癌的治疗一直是最难的。现在,在一项新的研究中,研究人员在宾夕法尼亚大学佩雷尔曼医学院照亮这癌症的一个主要的耐药机制:一种炎症所引起的肿瘤对治疗的反应,帮助保持肿瘤细胞的活力。
阻止这种炎症后放射治疗带来了显著改善生存在一个疾病的小鼠模型。
“这是一个进步的理解胰腺癌的电阻标准疗法,”首席研究员格雷戈里·比蒂说,医学博士,血液学/肿瘤学副教授潘和佩恩艾布拉姆森癌症中心的一员。该研究结果发表在1月的问题临床癌症研究。
强烈的抵抗治疗一直胰腺癌列表的顶部附近最致命的癌症。只有约百分之八的患者诊断为胰腺癌的常见类型cancer-pancreatic导管adenocarcinoma-survive另一个五年。在美国,每年大约有40000人,和世界各地超过300000人死于这种形式的癌症。
研究近年来,比蒂的实验室和其他人指出,这种治疗耐药性的一个潜在来源:胰腺肿瘤倾向于任用一个保护性的“微环境”。
“我们知道,如果你把这些肿瘤细胞的耐心,把它们放在培养皿中,它们可以被化疗,”比提说。“但在体内,在他们创造的微环境,他们甚至设法抵制消除我们的大多数细胞毒性治疗。”
这tumor-protecting微环境包括炎症白细胞单核细胞和巨噬细胞。在胰腺癌,他们的活动增加肿瘤的生长和传播,也可以帮助抑制T细胞和其他免疫元素,否则攻击肿瘤。
早期临床研究的另一个机构,发表在《柳叶刀肿瘤学2016年5月,块CCR2实验性的药物联合化疗,对单核细胞和巨噬细胞的激活受体刺激这些细胞渗透到肿瘤。虽然这项研究是小,结果承诺:阻塞CCR2导致更好的肿瘤反应相比单独化疗。
为他们的新研究,比蒂和同事测试了类似inflammation-blocking策略,结合放疗。辐射是经常用来治疗胰腺肿瘤没有传播,但不能被移除手术。
该研究的第一作者是Anusha Kalbasi医学博士当时放射肿瘤学居民宾夕法尼亚大学医学。Kalbasi现在临床讲师加州大学洛杉矶医学院。在小鼠胰腺肿瘤、Kalbasi和团队的其他成员发现相对较高水平的炎症化合物包括CCL2,激活CCR2在单核细胞和巨噬细胞的信号分子,使这些细胞迁移到肿瘤。大剂量放射治疗后,与人类患者接受什么,CCL2水平上升甚至更高,高得几次科学家发现,它是由肿瘤细胞分泌的。
“他们死在应对辐射,这是导致他们释放这些化学信号,呼叫帮助,然后让他们重生,”比提说。
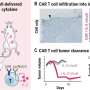
肿瘤的招募这些炎症细胞从而使他们能够抵抗原本已经致命剂量的辐射,所以,他们的增长放缓仅略有控制老鼠相比,没有收到任何辐射。相比之下,当团队小鼠辐射+ CCL2-blocking抗体治疗,肿瘤的招聘的单核细胞和巨噬细胞急剧减少,肿瘤增长大幅放缓更多。”的结合,不仅辐射和CCL2-blockade肿瘤生长缓慢,它长期生存在老鼠身上,“Kalbasi说。提高生存时间允许老鼠多活25%比单独处理辐射。
宾夕法尼亚大学科学家,调查结果表明,阻止CCL2-CCR2炎症通路在胰腺癌中值得调查作为一个附加放射治疗,不仅对化疗。根据这些原则,研究人员现在计划研究肿瘤相关炎症细胞和响应之间的关系在人类胰腺癌放射治疗病人。
“我们会发现病人更多的回应放射治疗是那些肿瘤产生更少的CCL2,从而减少招聘tumor-protecting单核细胞和巨噬细胞,”比提说。“如果是这样的话,这将是有用的识别这类患者在临床设置,因为他们可能受益于辐射在缺乏CCR2或CCL2抑制剂”。
但是他警告说,即使是radiation-plus-CCL2-blocking策略探索在新的研究中“不治愈mice-there仍然要做。”
特别是,虽然发现了其他一些癌症的放射治疗方案释放由病人的t细胞抗肿瘤反应,研究小组发现在他们的胰腺癌模型没有这样的效果。因此,可能有其他耐药机制,阻止胰脏cancer-mechanisms的抗肿瘤免疫反应,当他们更好的了解,可以有针对性的对未来药物允许抗肿瘤免疫的工作在这种致命的癌症。
“我们仍在试图找出为什么这些t细胞抗肿瘤不进入胰腺肿瘤像其他恶性肿瘤,”比提说。