大鼠生长的小鼠胰腺有助于逆转小鼠的糖尿病

东京大学斯坦福大学的研究人员说,大鼠生长的小鼠胰腺有助于逆转小鼠的糖尿病
在大鼠体内生长的小鼠胰腺产生功能性的,胰岛素生产细胞根据斯坦福大学医学院和东京大学医学科学研究所的研究人员的说法,当移植到患有糖尿病的老鼠身上时,可以逆转糖尿病。
受体动物只需要几天的免疫抑制治疗来防止基因匹配的排斥反应,而不是终身治疗。
跨物种移植的成功表明,类似的技术有一天可以用来生成匹配的、可移植的人体器官像猪或羊这样的大型动物。
为了进行这项工作,研究人员植入了老鼠多能干细胞这种细胞可以变成体内的任何细胞,变成早期大鼠胚胎。经过基因改造的大鼠无法发育自己的胰腺,因此被迫依赖小鼠细胞来发育该器官。
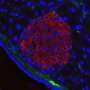
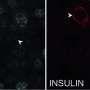
一旦老鼠出生和长大,研究人员就会移植产生胰岛素的细胞,这些细胞聚集在一起,称为小岛从大鼠生长的胰腺到基因匹配的小鼠干细胞这就形成了胰腺。这些老鼠服用了一种药物,使它们患上糖尿病。
斯坦福大学遗传学教授Hiromitsu Nakauchi博士说:“我们发现,在移植了100个胰岛后,糖尿病小鼠的血糖水平能够恢复正常一年多。”“此外,接受移植的动物只需要在移植后5天内接受免疫抑制药物治疗,而不需要对不匹配的器官进行持续的免疫抑制。”
中内是斯坦福大学干细胞生物学和再生医学研究所的成员,他是一篇描述这一发现的论文的高级作者,该论文将于1月25日在网上发表自然.来自东京大学的干细胞治疗副教授Tomoyuki Yamaguchi博士和研究员Hideyuki Sato共同是这篇论文的主要作者。
器官供应不足
目前,美国约有76000人在等待器官移植,但器官供不应求。研究人员说,在大型动物身上制造基因匹配的人体器官可以缓解这种短缺,并使移植受者摆脱终身免疫抑制的需要。
糖尿病患者也可以从这种方法中受益。糖尿病是一种危及生命的代谢性疾病,患者或动物无法制造或对胰岛素做出适当的反应,胰岛素是一种让身体调节胰岛素的激素血糖水平对正餐或禁食的反应。这种疾病影响着全世界数亿人,而且发病率正在上升。健康胰腺的功能胰岛移植已被证明是治疗人类糖尿病的潜在可行选择,只要可以避免排斥反应。
研究人员目前的发现紧随之前的一项研究,他们在小鼠体内培养了大鼠胰腺。尽管这些器官看起来功能正常,但它们的大小与正常小鼠的胰腺相当,而不是大鼠的胰腺。结果,在较小的器官中没有足够的功能胰岛来成功逆转大鼠的糖尿病。
在大鼠体内生长的小鼠胰腺
在目前的研究中,研究人员交换了动物的角色,在经过改造后缺乏胰腺的大鼠体内培养小鼠胰腺。胰腺能够成功地调节大鼠的血糖水平,表明它们的功能正常。大鼠的免疫系统对小鼠胰脏的排斥反应并不常见老鼠的细胞在大鼠胚胎产生免疫耐受之前注射到大鼠胚胎中,免疫耐受是发育过程中的一个时期,免疫系统被训练来识别自己的组织为“自我”。这些来源于小鼠的器官大多长到大鼠胰腺的大小,产生足够的个体胰岛供移植。
接下来,研究人员将100个大鼠胰岛移植回患有糖尿病的小鼠体内。随后,研究人员发现,这些小鼠能够成功地控制他们的血糖水平超过370天。
因为移植的胰岛含有一些污染的大鼠细胞,研究人员在移植后用免疫抑制药物治疗每只受体小鼠五天。然而,在此之后,免疫抑制停止了。
大约10个月后,研究人员从一部分小鼠中取出胰岛进行检查。
“我们仔细检查了它们是否存在大鼠细胞,但我们发现老鼠的免疫系统已经消除了它们,”中内说。“这对我们移植动物体内生长的人体器官的希望非常有希望,因为它表明,移植后,任何污染的动物细胞都可以被患者的免疫系统清除。”
重要的是,研究人员也没有发现任何由形成胰岛的多能性小鼠干细胞引起的肿瘤形成或其他异常的迹象。当多能干细胞用于动物时,由于细胞具有显著的发育可塑性,肿瘤形成往往是一个问题。研究人员认为,没有任何癌症迹象可能是由于小鼠多能干细胞在发育中的大鼠胚胎中被引导生成胰腺,而不是在实验室中被诱导发育成胰岛细胞。研究人员正在进行类似的动物间实验,以生成肾脏、肝脏和肺。
虽然这些发现为未来的工作提供了原理证明,但仍有许多研究要做。当人类干细胞移植到动物胚胎时,伦理考虑也很重要研究人员承认。
进一步探索