诊断癌症:确定生物标记物的新方法

Ruhr-Universität波鸿的科学家已经建立了一种识别不同类型癌症诊断的生物标志物的过程。在一种特定类型的红外光谱技术的帮助下,研究人员应用了一种自动化和无标签的方法来检测活体组织或组织样本中的肿瘤组织。与病理学家目前使用的基于标签的过程不同,组织仍然未被修改。这反过来又促进了下一步详细的蛋白质分析。研究人员研究了肺癌或胸膜癌患者的组织样本,确定了各自癌症亚型的典型蛋白质生物标志物。
“欧洲鲁尔区蛋白质研究单位”(PURE)研究联盟的团队在《欧洲科学》杂志上发表了他们的报告。科学报告”。
建立具体的工作流程
通过他们目前的工作,来自波鸿的研究人员将他们对PURE的愿景完全付诸实践。PURE发言人Klaus Gerwert教授解释说:“这是第一次完全重现了从一开始就计划好的工作流程。”在这个过程中,新鲜组织立即冷却,然后带到研究中心并记录在案。之后,进行传统的诊断,这是每个患者的标准,同时使用在波鸿进行的过程进行分析。
为了研究的目的,研究人员对所谓的弥漫性恶性间皮瘤组织样本进行了研究。他们比较了间皮瘤的两种亚型——肉瘤样和上皮样。这种类型的癌症通常散入肺部,通常是晚期。
波鸿制造的诊断过程
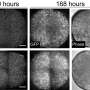
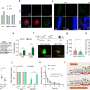
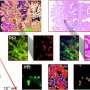
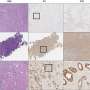
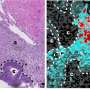
研究人员用高空间分辨率的红外显微镜描绘了肿瘤的扩散。Klaus Gerwert和Frederik Großerüschkamp博士在PURE的保护下开发了这种成像方法。这使他们能够区分不同亚型的癌症——这是预后和治疗的重要信息。它不需要任何染料或抗体,这在传统病理学中是必要的。由于组织未经过修饰,因此可以随后在分子水平上分析相同的样本。
在肿瘤定位后组织样本在美国,研究人员使用特殊的激光技术将其切割出来。在Medizinisches蛋白质中心(Ruhr-Universität),同样是PURE联盟的成员,由Barbara Sitek教授和Katrin Marcus教授领导的专家们使用质谱分析提取组织的蛋白质组成。
个性化诊断
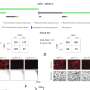
因此,研究人员能够确定与上皮样间皮瘤相比,肉瘤样间皮瘤中2000多种已鉴定的蛋白质中哪些明显增加或减少。“因此,我们可以确定每个患者癌细胞信号转导的变化,”Klaus Gerwert解释说。“这是精确治疗的关键信息。”
这样鉴定出的蛋白质将来可能被用作生物标志物,以检测其他患者的癌症类型。研究人员研究了检测到的蛋白质和目前在传统病理学中使用的生物标志物之间的相关性。结果:在波鸿制作的方法还识别了已经用于诊断间皮瘤亚型的五种生物标志物。“因此,我们已经验证了我们的方法,”Gerwert解释说。纯研究人员还发现了其他生物标志物。Gerwert:“这些生物标志物还有待于下一步在更大的队列中进行验证。”
Frederik Großerüschkamp说:“目前,新开发的无标签方法是独一无二的,它开辟了在未来专门搜索生物标志物的可能性。”
目标是在体液中找到生物标记物
Gerwert和他的同事打算将这种方法应用于其他类型的癌症,从而识别新的生物标志物。生物物理系的负责人概述了一个前景:“我们的目标是检测我们现在在组织和体液(如血液和尿液)中发现的生物标记物,”Gerwert说。“这将有助于通过简单的抗体测试进行非侵入性、精确和预测性的诊断。”
弥漫性恶性间皮瘤
弥漫性恶性间皮瘤主要是由于接触石棉引起的。肿瘤的形式非常多样,而且受影响的人数相对较少,这使得研究相当困难。“特别是在这种情况下,我们的新方法可能会提供一种有价值的替代方案生物标志物Großerüschkamp解释道。
更多信息:Frederik Großerueschkamp等人,通过整合无标签FTIR成像,激光捕获显微解剖和蛋白质组学,弥漫性恶性间皮瘤异质性的空间和分子分辨率,科学报告(2017)。DOI: 10.1038 / srep44829