研究人员将脑血管病变与肠道细菌联系起来
一项对小鼠和人类的研究表明,肠道中的细菌可以影响大脑血管的结构,并可能导致导致中风或癫痫的畸形。这项发表在《自然》杂志上的研究进一步揭示了肠道微生物和神经系统紊乱之间的联系。这项研究是由美国国立神经疾病和中风研究所(NINDS)资助的,该研究所是美国国立卫生研究院的一部分。
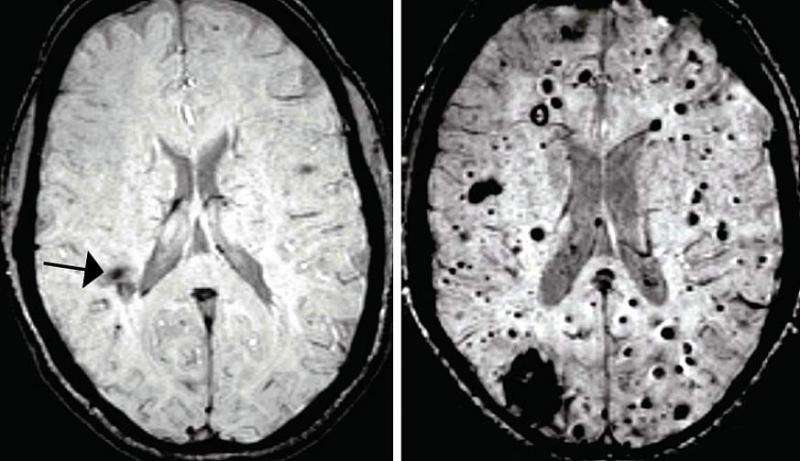
脑海绵状畸形(CCMs)为扩张的薄壁簇状血管当血液渗入周围脑组织时,可能导致癫痫或中风。宾夕法尼亚大学的一组科学家研究了导致CCM损伤形成的基因工程小鼠的机制,并发现了一个意想不到的联系细菌在肠道。当细菌被消除时,病变的数量大大减少。
“这项研究令人兴奋,因为它显示了体内的变化可以影响由基因突变引起的疾病的进展,”吉姆·i·凯尼格博士说,他是NINDS的项目主管。
研究人员正在研究一个成熟的小鼠模型,该模型在注射药物诱导基因缺失后会形成大量的ccm。然而,当动物被转移到一个新的设施,病变形成的频率下降到几乎为零。
“这完全是个谜。突然间,我们正常可靠的小鼠模型不再形成我们预期的病变,”Mark L. Kahn医学博士说,他是宾夕法尼亚大学医学教授,也是该研究的资深作者。“有趣的是,这种病变形成的差异性也见于人类,具有相同基因突变的患者往往有显著不同的病程。”
在调查这种突然变化的原因时,Kahn博士实验室的研究生Alan Tang注意到,少数继续形成病变的小鼠的腹部出现了细菌脓肿——这种感染很可能是由于腹腔注射药物引起的。脓肿中含有革兰氏阴性细菌,当在CCM模型动物中故意诱导类似的细菌感染时,大约一半的脓肿出现显著的CCM。
“形成ccm的小鼠的脾脏中也有脓肿,这意味着细菌已经从最初的脓肿部位进入了血液,”唐说。“这表明一种特定类型的细菌通过血液的传播与大脑中这些血管病变的形成之间存在联系。”
问题仍然是,血液中的细菌如何影响大脑中的血管行为。革兰氏阴性细菌产生脂多糖(LPS)分子,是先天性免疫信号的有效激活剂。当小鼠只接受LPS注射时,它们形成了大量的大型ccm,与细菌感染产生的ccm类似。相反,当LPS受体TLR4从这些小鼠的基因中移除时,它们不再形成CCM病变。研究人员还发现,在人类中,基因突变引起TLR4表达的增加与形成ccm的更大风险相关。
“我们知道病变的形成可能是由体内的革兰氏阴性细菌通过LPS信号驱动的,”Kahn说。“我们的下一个问题是,我们是否可以通过改变体内的细菌来预防病变。”
研究人员通过两种方式探索人体细菌(微生物组)的变化。首先,新生CCM小鼠在正常住房或无菌条件下饲养。其次,给这些老鼠一个疗程的抗生素来“重置”它们的微生物群。无论在无菌条件下还是在抗生素疗程后,数量病变显著降低,说明肠道微生物群的数量和质量都能影响CCM的形成。最后,一种专门阻断TLR4的药物也产生了显著的减少病变的形成。该药物已经在治疗脓毒症的临床试验中进行了测试,这些发现表明该药物在治疗CCMs方面具有治疗潜力,尽管还有相当多的研究有待完成。
Koenig说:“这些结果特别令人兴奋,因为它们表明我们可以将在老鼠身上的发现应用于人类患者群体。”“用于阻断TLR4的药物已经在其他疾病的患者中进行了测试,它可能在CCMs的治疗中显示出治疗潜力,尽管仍有大量的研究要做。”
Kahn和他的同事计划继续研究微生物组和CCM形成之间的关系,特别是它与人类疾病的关系。虽然已经在人类中发现了导致ccm形成的特定基因突变,但具有相同突变的患者ccm的大小和数量差异很大。该小组下一步的目标是检验一个假设,即患者微生物组的差异可以解释病变数量的变化。
进一步探索













用户评论