干细胞提前将生物工程更接近现实
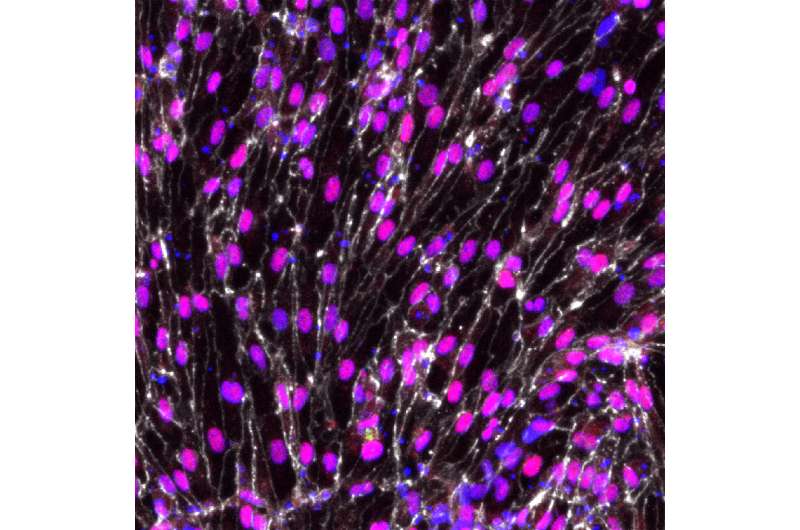
干细胞生物学家多年来一直试图制造出能够形成动脉功能的细胞,并为医生们提供新的治疗心血管疾病的选择,但都以失败告终。心血管疾病是世界上最主要的死亡原因。
但是,莫里奇研究所和威斯康星大学麦迪逊分校开发的新技术第一次产生了在质量和规模上与疾病建模和临床应用相关的功能动脉细胞。
发表在7月10日的杂志上美国国家科学院院刊干细胞先驱詹姆斯·汤姆森实验室的科学家们描述了产生和表征动脉内皮细胞的方法。血管内皮细胞是启动动脉发育的细胞,具有许多人体所需的特定功能。
此外,这些细胞有助于新动脉的形成和提高小鼠的存活率用于心肌梗死模型。用这种细胞系治疗的小鼠存活率为83%,而对照组为33%。
“致人死亡的心血管疾病主要影响动脉Morgridge的助理科学家和主要作者张珏(Jue Zhang)说。“这里的关键发现是一种使动脉内皮细胞更有功能和临床用途的方法。”
根据美国心脏协会(American Heart Association)的数据,在美国,每年死于心血管疾病的人占死亡人数的三分之一,而且每年死于心血管疾病的人比死于各种癌症的人加起来还要多。汤姆森实验室将动脉工程作为其研究重点之一。
Zhang说,挑战在于一般内皮细胞相对容易制造,但它们缺乏真正的动脉特性,因此没有什么临床价值。

该研究团队在该项目中应用了两项开创性技术。首先,他们使用单细胞RNA测序来识别对动脉内皮细胞分化至关重要的信号通路。他们发现了大约40个最佳相关性的基因。其次,他们使用CRISPR-Cas9基因编辑技术,使他们能够创建报告细胞系,实时监测动脉分化。
“有了这项技术,你可以测试这些候选基因的功能,并测量有多少百分比的细胞生成我们的目标动脉细胞,”张说。
研究小组围绕对动脉细胞发育贡献最大的五种关键生长因子开发了一种协议。他们还发现了一些在干细胞科学中使用的非常普遍的生长因子,如胰岛素,令人惊讶地抑制了动脉内皮细胞的分化。
“我们的最终目标是将这种改进的细胞衍生过程应用于可用于心血管外科手术的功能性动脉的形成,”摩根里奇再生生物学主任、威斯康辛大学麦迪逊分校细胞和再生生物学教授汤姆森说。“这项工作提供了有价值的证据,证明我们最终可以获得可靠的功能动脉内皮细胞来源,并使动脉的运行和行为像真实的东西。”
汤姆森的团队与威斯康辛大学麦迪逊分校的许多合作者一起,正在进行一个由美国国立卫生研究院(NIH)资助的为期7年的项目的第一年,该项目旨在研究开发适合用于人体移植的动脉银行的可行性。
在许多血管疾病的病例中,患者缺乏适合自己身体的组织用于搭桥手术。以及一个病人的动脉干细胞将是成本持有的并且需要太长的临床上有用。
挑战将不仅仅是制造动脉,还要找到方法来确保它们是兼容的,不会被病人排斥。
“现在我们有了一种创造这些细胞的方法,我们希望用一种更通用的供体细胞系继续努力,”张说。实验室将专注于细胞银行从一个独特的人群中建立他们是大多数人的基因兼容捐赠者。
进一步探索












用户评论