卵巢癌难治亚型的新治疗方法
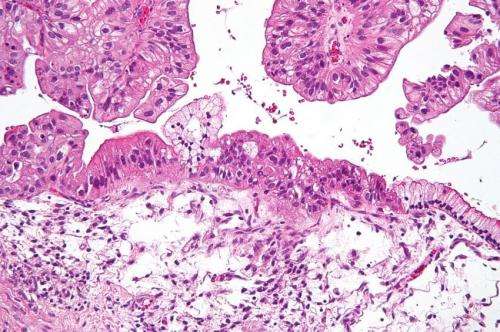
威斯塔的科学家们发现了一种治疗一种难以治疗的卵巢癌的新方法。研究结果发表在自然细胞生物学。
在美国,卵巢透明细胞癌约占5%到10%卵巢癌在亚洲,这一比例约为20%,是导致卵巢癌死亡的第二大原因癌症。透明细胞亚型的患者通常对铂类化疗反应不佳,给这些患者留下有限的治疗选择。
以前的研究包括在Wistar学院进行的那些,揭示了Arid1a,染色质重塑蛋白在该卵巢癌亚型中的作用。当正常工作时,ARID1A通过改变染色质的结构 - DNA和蛋白质的复合物在我们的细胞中进行调节某些基因的表达。这个过程决定了一些细胞的行为,并阻止他们成为癌症。
“常规化疗已被证明是治疗这一组卵巢癌患者的无效手段,这意味着必须探索基于一个人的基因组成的替代策略,”张汝刚博士说。Wistar's Gene Expression and Regulation Program的教授和合作项目负责人,也是本研究的通讯作者。“基于ARID1A突变的治疗方法有可能彻底改变我们治疗这些患者的方式。”
最近的研究表明,在超过50%的卵巢透明细胞癌病例中,ARID1A会发生突变。ARID1A和肿瘤抑制基因TP53是相互排斥的,这意味着ARID1a突变的患者尚不携带TP53的突变。尽管如此,TP53的功能可以保护我们基因组完整性并促进编程的细胞死亡,显然是疾病患者的预后差。
在本研究中,Zhang和同事研究了ARID1A和组蛋白去乙酰化酶(HDACs)之间的联系,HDACs是一组参与关键生物学功能的酶。他们发现,HDAC6活性在arid1a突变的卵巢癌中至关重要。他们能够证明,HDAC6通常被ARID1A抑制,而在ARID1A突变的情况下,HDAC6水平上升。由于HDAC6抑制TP53的活性,从而抑制其抑瘤功能,高水平的HDAC6允许肿瘤生长和扩散。
使用叫做罗氏菌蛋白酶的小分子药物,可选择性地抑制HDAC6,张实验室发现,通过阻断ARID1A突变的癌症中酶的活性,它们能够仅在那些肿瘤中增加细胞凋亡或编程的细胞死亡细胞含有ARID1A突变。这与显着的减少相关瘤生长,抑制腹膜传播和携带ARID1A突变卵巢肿瘤的动物模型存活的延长。
“我们证明,使用像罗氏菌蛋白酶等选择性抑制剂的靶向HDAC6活性代表治疗卵巢透明细胞癌等可能的治疗策略和受突变的ARID1A影响的其他肿瘤,”Zhang Lab和博士后的博士学位该研究的联合第一作者。“抑制剂,我们在本研究中使用的抑制剂在临床试验中得到了良好的耐受性,因此我们的研究结果可能具有深远的应用。”
进一步探索













用户评论