有缺陷的支持细胞扰乱精神分裂症的脑中的沟通
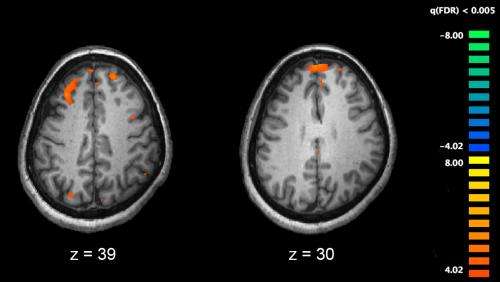
新的研究已经确定了精神分裂症患者大脑的布线问题背后的罪魁祸首。当研究人员移植从被诊断患有儿童出血精神分裂症的个体生成的人脑细胞进入小鼠时,动物的神经细胞网络没有适当成熟,小鼠表现出与疾病的人们相同的反社会和焦虑行为。
"The findings of this study argue that glial cell dysfunction may be the basis of childhood-onset schizophrenia," said University of Rochester Medical Center (URMC) neurologist Steve Goldman, M.D., Ph.D., co-director of the Center for Translational Neuromedicine and lead author of the study which appears today in the journal细胞。“这些细胞无法做到他们的工作,这是为了帮助神经细胞建立和维持健康和有效的通信网络,似乎是疾病的主要贡献者。”
Glia是大脑中发现的重要支持细胞系列,并在大脑复杂的神经元网络的开发和维护中发挥着关键作用。Glia包括两种主要类型:星形胶质细胞和oligodendrocytes。星形胶质细胞是大脑的主要支持细胞,而少突胶质细胞负责生产髓鞘,脂肪组织,如电线上的绝缘,包裹连接不同神经细胞的轴突。两种细胞的来源是另一种称为胶质祖细胞(GPC)的细胞类型。
星形胶质细胞在大脑中执行若干功能。在开发期间,星形胶质细胞殖民地的脑和建立这些细胞有助于直接和组织神经细胞之间连接网络的结构域。个体星形胶质细胞也发出了数百个长纤维,与突触相互作用 - 一个神经元轴突与另一个人的树突相遇的交界处。星形胶质细胞通过调节谷氨酸和钾的流动,有助于突触在突触中的神经元之间的沟通,这使得当它们彼此通信时使神经元成为“火”。
在新的研究中,研究人员获得了具有儿童发病精神分裂症的个体的皮肤细胞,并重新编程细胞以产生诱导的多能干细胞(IPSC),如胚胎干细胞,能够产生身体中发现的任何细胞类型。雇用首次由高盛实验室开发的过程,该团队操纵了IPSC来创建人类GPC。
然后将人的GPC移植到新生小鼠的大脑中。这些细胞从动物自己的原生胶质群体中竞争,导致患有动物神经元和人类GPC,少突胶质细胞和星形胶质细胞组成的小鼠。
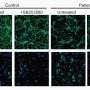
研究人员观察到来自精神分裂症患者的人类神经胶质细胞具有高度功能障碍。少突胶质细胞的发展延迟,细胞没有产生足够的髓鞘细胞,这意味着神经元之间的信号传递受损。
星形胶质细胞的发展类似地迟钝,因此在需要时不存在细胞,因此在引导神经元之间的连接形成方面不效应。星形胶质细胞也没有正常成熟,导致畸形细胞不能完全支持周围神经元的信号功能。
“星形胶质细胞并没有完全成熟,他们的纤维没有填满他们的正常域,这意味着他们向某些突触的控制提供了控制,其他人没有覆盖,”威尔斯·温雷姆(Martha Windrem)表示,urmc的翻译神经核细节和第一个作者在这项研究中。“结果,动物中的神经网络变得了不协调的。”
研究人员还将小鼠与一系列行为测试进行。他们观察到,来自诊断出精神分裂症的人类人类神经胶质细胞的小鼠更加恐惧,焦虑,反社会,与移植的小鼠相比,与从健康人的人类神经胶质细胞移植的小鼠相比,具有各种认知缺陷。
该研究的作者指出,新的研究为科学家提供了探索疾病的新治疗的基础。因为精神分裂症是人类独有的,直到现在科学家们在学习疾病的能力中受到限制。开发研究人员的新动物模型可用于加速精神分裂症中的药物和其他疗法的过程。该研究还确定了许多胶质基因表达缺陷,似乎产生了破坏神经元之间的沟通的化学不平衡。这些异常可能代表新疗法的目标。
进一步探索










用户评论