产前缺乏ω-3和ω-6脂肪酸与小鼠的精神分裂症症状联系起来
日本riken脑科学研究所的研究人员发现了一种过程,早期鼠标妊娠期间的营养变化导致后代,将精神分裂症样症状发展为成年人。出版于翻译精神病学该研究表明,在早期妊娠期间,如何剥夺两种多不饱和脂肪酸可以通过基因表达的特异性表观遗传变化对后代的持久影响。
众所周知,怀孕期间的有害条件会影响后代的健康,甚至导致成人发病的疾病。这个概念——健康与疾病的发展起源(DOHaD)——可以解释为什么观察到精神分裂症的发病率在饥荒后翻倍。为了开发有效的精神分裂症治疗方法,吉川武夫和他在日本理化研究所的团队正在研究早期营养不良是如何改变精神分裂症的大脑。
第一作者Motoko Maekawa指出,“我们的工作是精神病学领域的第一个,以确定将营养环境与Dohad Paradigm的背景中联系在疾病风险中的分子级联。”
弄清楚“如何”的第一步是确定最有可能的营养素,其缺乏与精神分裂症有关。在与精神分裂症相关的几个候选人中,团队选择研究两种特定的多不饱和脂肪酸-3脂肪酸DHA和-6脂肪酸aa -因为它们在大脑中大量存在,众所周知,它们与大脑发育有关。研究小组通过剥夺怀孕小鼠的DHA和AA来验证他们的理论,并测试它们的成年后代是否具有精神分裂症患者所表现出的特征。
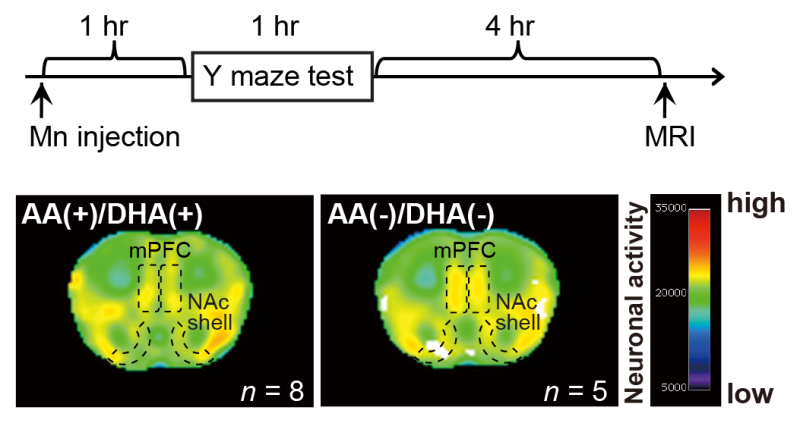
精神分裂症早期患者有几种常见症状,包括低动力、抑郁、记忆受损和脑功能异常前额外的皮质。母亲被剥夺了DHA和AA的成年小鼠表现出类似的症状。
由于前额叶皮层中的功能障碍是精神分裂症的标志,该团队接下来研究了DHA / AA剥夺如何影响大脑的那部分中的基因表达。在数百人受影响中基因他们发现精神分裂症患者的一组基因表达下调,而受影响的小鼠的基因表达也出现了下调。这些基因与少突胶质细胞有关,少突胶质细胞是大脑中包围神经元的细胞,有助于大脑中的信号传递。此外,影响GABA神经递质系统的基因表达改变的方式模仿了精神分裂症患者死后大脑的发现。
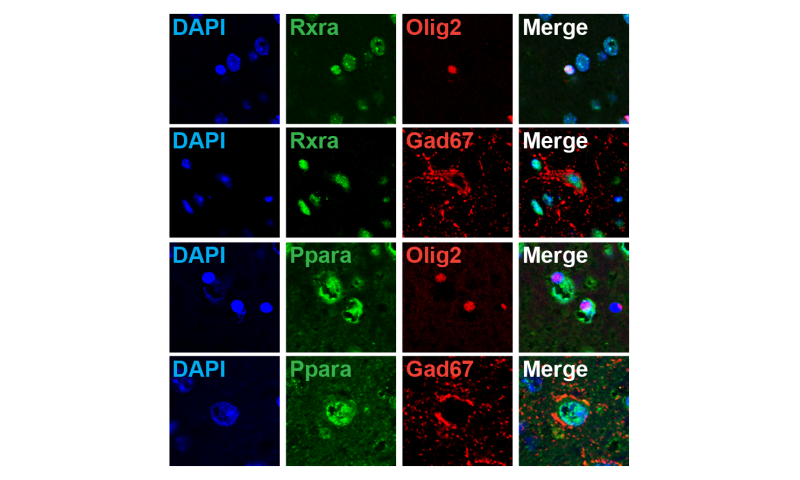
基因表达可以通过某种叫做核受体的蛋白质来控制,该蛋白质附着于DNA,并引发从DNA码中构建蛋白质的转录过程。当团队进行进一步分析脂肪酸被剥夺的小鼠时,他们发现已经下调了与脂肪酸有关的几种核受体基因。事实证明,少突胶质细胞相关基因的异常表达可以直接追溯到这些核受体的低表达,这又可以追溯到更高水平的DNA甲基化,一种调节基因表达的常见方法。通过这种方式,改变的饮食成功地创造了持久的变化基因表达。
一旦他们知道下调哪种核受体基因,该团队可以考虑如何扭转该过程。当他们赋予对小鼠作用于RXR核受体的药物时,它们发现上调少突相关基因,并且一些异常的电机行为减少。“这证明了作用于核受体的药物可以是精神分裂症的新疗法,”Maekawa说。
了解负责的基因也使团队成为患有精神分裂症的人的目标。两种单独的精神分裂症患者的毛囊分析表明它们也表现出降低表达相同的核受体基因“下一步,”前川解释说,是测试针对这些核武器的药物的有效性受体患者的精神分裂症,并调查如何核受体调节少突胶质细胞和GABAergic神经元的功能,以防止精神分裂症病理生理的发展。”
进一步探索








用户评论