研究人员揭示了用于引导前列腺癌治疗的生物标志物
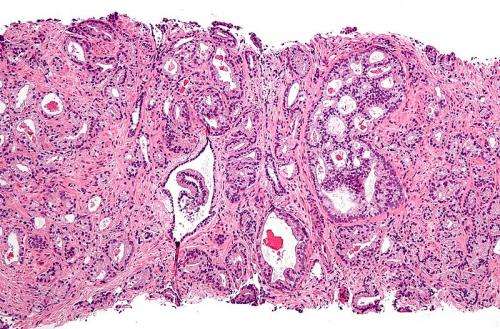
来自克利夫兰诊所的背靠背发现首次证明了睾酮相关的遗传异常如何有助于预测对特异性前列腺癌疗法的个体患者的反应。
这项研究发表在10月12日的《科学》杂志上贾马肿瘤学,建议继承这个的男人变体将受益于针对特定激素途径的个性化治疗计划。
由克利夫兰诊所拉尼尔研究院的Nima Sharifi,M.D.的研究小组研究了HSD3B1(1245C)遗传变异在两种不同前列腺癌患者群体中的作用,如下雄激素剥夺疗法(ADT)。ADT通过阻断前列腺癌睾丸中雄性激素的供应而起作用。它是复发性前列腺癌的基础治疗方法,但它经常停止工作,让癌症进展和扩散。2013年,沙里菲博士发现,具有遗传异常的前列腺癌细胞通过产生自身的雄激素而存活于ADT。
在第一项新研究中,纪念斯洛安凯特宁癌症中心的Sharifi博士和同事们,哈佛/达纳 - 前癌症学院和密歇根大学综合癌症中心分析了213名男子前列腺癌,在放射治疗和接受ADT后复发。他们在辐射和ADT之后第一次找到了,前列腺在携带HSD3B1(1245C)变异的男性中,癌症更容易扩散,而且扩散速度更快。
第二项研究与加州大学旧金山大学的研究人员进行了审查了一组90名男子转移癌症这对ADT具有抵抗力。随后将这些患者用药物酮康唑处理,该酮酮阻断睾丸外的雌激素(例如,由前列腺癌细胞这是逃避ADT治疗)。
令人惊讶的是,有基因异常的男性服用酮康唑比没有这种变异的男性表现更好。这一发现提出了一种可能性,即当ADT失败时,靶向变异肿瘤的备用雄激素供应(睾丸外)可能是一种成功的策略。
Sharifi博士说:“我们假设HSD3B1(1245C)变体肿瘤对ADT产生耐药性是因为它们有备用的雄激素供应。”“然而,依赖这些性腺外雄激素使他们对酮康唑更敏感。”
这些发现补充了早期的研究,并支持使用HSD3B1(1245C)作为预测生物标志物,以帮助指导关键治疗决策。虽然这种基因变异患者的前景差,但这些研究为这些男性的新治疗策略提供了希望,并且需要使用下一代雄激素抑制剂,例如AbiraTerone和烯醇酰胺。
“我们希望这些发现将导致更个性化和有效的治疗前列腺癌沙里菲博士说。“如果男性携带一种特定的睾丸激素相关的基因异常,我们可能会对他们的治疗进行个性化,对特定的患者进行更积极的治疗。”
Sharifi博士也是Glickman泌尿科学院和克利夫兰诊所塔斯格癌症研究所的成员。他拥有克利夫兰诊所的前列腺癌研究肯德里克家族椅,并共同指导克利夫兰诊所的前列腺癌研究中心。2017年,他获得了临床研究论坛的十大临床研究成就奖,即他的地标发现,携带HSD3B1(1245C)变异的男性更有可能死于他们的疾病。











用户评论