抗癌药物开始在人类脑癌患者身上进行临床试验

一种刺激癌细胞自我毁灭的药物已被批准用于癌症治疗临床试验患有间变性星形细胞瘤(一种罕见的恶性脑瘤)和多形性胶质母细胞瘤(一种侵袭性晚期脑癌)的患者。这项Ib期试验将确定实验性药物PAC-1是否可以与标准的脑癌化疗药物替莫唑胺联合使用。
该试验被批准用于一线治疗后癌症进展的患者。这是一个正在进行的人类的延伸一期临床试验PAC-1在各种晚期癌症患者中的作用第一阶段试用旨在测试新药在人类患者身上的安全性。
PAC-1的不同寻常之处在于它能够穿过血脑屏障,而血脑屏障是大多数抗癌药物的巨大障碍。这种药物的目标是procaspase-3,这是一种在许多细胞中过表达的酶癌症细胞伊利诺伊大学化学教授保罗·赫根罗瑟(Paul Hergenrother)说,他在十多年前发现了PAC-1的抗癌作用。在对人类细胞系和啮齿动物的测试证明前景良好后,赫根罗瑟和伊利诺斯州兽医临床医学教授、兽医肿瘤学家蒂莫西·范博士对宠物的PAC-1进行了测试狗各种自然发生的癌症。
“大多数癌症都有procaspase-3水平升高,”Hergenrother说。“当它被打开时,procaspase-3会杀死它细胞."
然而,他说,癌细胞会覆盖正常的细胞循环途径。
他说:“PAC-1恢复procaspase-3的激活,并且由于这种酶在癌细胞中升高,针对癌细胞而不是非癌细胞。”
PAC-1已经在患有自然发生的骨肉瘤、淋巴瘤和最近的胶质瘤(一种类似于人类胶质母细胞瘤的脑癌)的宠物狗身上进行了评估。一个2016年的研究发现PAC-1与阿霉素(一种也用于人类的化疗药物)的组合,在4只患有淋巴瘤的狗中有4只,在6只患有骨肉瘤的狗中有3只。在狗身上的试验仍在继续,到目前为止,已经发现PAC-1是安全的,除了偶尔的胃肠不适外,几乎没有明显的副作用。研究人员报告他们在啮齿类动物和患有脑癌的狗身上的最新发现发表在杂志上Oncotarget.
范说,患有某些自然发生的癌症的狗可能比其他人类癌症的动物模型更好,因为许多癌症药物测试模型中使用的小鼠和大鼠必须植入人类癌细胞来模拟特定类型的肿瘤。
他说:“这要求啮齿动物的免疫功能受损,以减轻对人类细胞的排斥反应。”“因此,大多数啮齿动物肿瘤模型并不能忠实地概括肿瘤微环境,特别是人体对肿瘤的免疫监测。
“啮齿动物模型是有限的,但它们仍然有用,”范说。
狗的某些癌症在基因上与人类相似,对相同的药物有反应。狗在体型上也与人类更相似,因此可以作为更好的模型来评估药物在较大肿瘤肿块上的效果。
“我把患有自发肿瘤的宠物视为啮齿动物模型的补充,并认识到并不是所有的发现都是如此宠物狗也必然适用于人类。”
医学肿瘤学家Arkadiusz Dudek博士说,正在进行的PAC-1在晚期实体瘤和淋巴瘤患者身上的临床试验表明,该药物在测试剂量高达每天450毫克时具有良好的耐受性临床试验.
他说,脑癌患者的I期试验将从每天375毫克的PAC-1剂量开始,并将逐步增加剂量,以测试其与标准的脑癌化疗药物替莫唑胺联合使用的安全性。
到目前为止,单独的PAC-1临床试验在人体上没有发现明显的副作用。研究人员报告说,在单药试验的前五个剂量水平中,没有一个人类患者因副作用而退出。研究小组不能报告I期临床试验的临床结果,因为这类试验的目的是衡量安全性,而不是疗效。
手术是间变性星形细胞瘤的一线治疗方法,其次是替莫唑胺,一种化疗药物,是为数不多的有效治疗方法之一脑癌杜德克说。人类与多形性成胶质细胞瘤通常进行手术,尽可能多地去除癌变组织,然后进行放疗和口服替莫唑胺治疗。
要发现并切除所有的胶质母细胞瘤几乎是不可能的癌症然而,Dudek说。
“多形性胶质母细胞瘤具有沿大脑内血管无声扩散的特征,”他说。“这就是为什么大多数患者在手术和放疗后不幸复发的原因。”
接受标准治疗的人类胶质母细胞瘤患者的中位生存时间约为15个月。
胶质瘤试验中的三只狗每天口服PAC-1,并结合替莫唑胺和“治疗性”辐射。
范教授说,替莫唑胺通常太贵,无法用于犬类患者。他说,这些狗对联合治疗的耐受性非常好,对治疗的反应也很好。
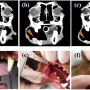
“至少,这三只狗都有我们所说的部分反应,这意味着肿瘤减少了30%以上,”他说。“其中一只狗有完全的反应,正如连续的核磁共振扫描所确定的那样,它的脑出血减少了100%肿瘤在联合治疗84天后发生肿块。”
范说,还需要在狗身上进行更大规模的研究,以确定治疗效果是否一致和可重复性,并量化PAC-1对积极结果的贡献。
Hergenrother在2011年帮助成立了一家药物开发初创公司Vanquish Oncology,该公司已从伊利诺伊大学(University of Illinois)获得了这项技术的许可,并致力于将PAC-1应用于临床。与任何研究药物一样,确定PAC-1的真正安全性和有效性将需要数年的人体临床试验。