新的治疗方向寻找帕金森通过阻断自然保护的拦截器

氧化应激中起着很大的作用的脑细胞损失发生在帕金森病。现在科学家们的目光投向一个蛋白质,抑制人体的自然保护。
Bach1拦截器,可以把蛋白和转录因子基因断断续续,大多了,保持不活跃的一些可以保护200个基因大脑细胞毁于帕金森氏症。
它应该工作的方式是高水平的氧化应激由于氧气使用,但生长在帕金森氏病,茎高危险激活蛋白Nrf2,进而激活这些基因。
但协同是在这种疾病,氧化应激和Bach1水平上升,所以应对压力的能力可能会下降。
“我们正在试图做的是恢复平衡,因为在这个疾病,失去了平衡,”博比·托马斯博士说,神经学系的药理学和毒理学在乔治亚州奥古斯塔大学医学院的。“一个办法是通过Bach1方程。”
托马斯最近收到了196万美元的赠款从美国国立卫生研究院的这部小说进一步追求治疗的目标脑退行性疾病诊断在每年大约60000美国人。他的发现到目前为止包括显示删除Bach1保护从帕金森病实验动物。
Nrf2通常发现本质上是不活跃的,绑定到一个叫做Keap1的蛋白质在细胞的液体部分称为胞质。氧化应激提示Keap1释放Nrf2,转移到细胞核,它可以激活200神经保护基因。但首先Bach1必须让开。
Bach1坐在监管区域,被称为抗氧化反应的元素,或阿瑞斯,这些基因,有效地抑制这些天生的保护者从氧化应激,托马斯说。虽然Bach1应该搬,在这种情况下的高氧化应激帕金森似乎压倒upregulation Nrf2。所以托马斯和他的团队正在把Bach1从方程与药物和基因操作。
在老鼠身上,他们已经表明,当他们减少Bach1,它提示不断激活以及没有得到基因也出现保护大脑甚至可以提供更多新的治疗目标。新NIH资助使他们能够了解更多关于释放的神经保护机制当Bach1消失了。
出现显著的能力。Bach1删除甚至防止毒素用于创建疾病的动物模型。现在他们正在探索Bach1扮演什么角色在神经元死亡的神经毒素,MPTP。他们也看着Bach1导致帕金森病的遗传形式的蛋白质α-突触核蛋白,发生在健康的大脑,也变得神经毒性。大量的α-突触核蛋白,称为路易小体,口香糖的神经元和支持工作细胞疾病的一个标志。
在实验室动物失踪Bach1,托马斯的团队观察药物直接激活Nrf2,开车好基因的表达甚至更高。托马斯也正在探索一个相当令人意外的是,当Bach1和Nrf2都消除,优良基因在某种程度上仍然被激活,提供更多的证据表明,其他基因也必须参与,可以提供更多新颖的目标,他说。例如,他的实验室已经记录了各种保护的重要upregulation基因的差别,对这些基因的其他人,如肿瘤坏死因子α,最终促进炎症和创造更多的氧化应激。
很明显,一些自然补偿机制是在工作中即使疾病发生,他说,因为,至少在后期的帕金森患者的大脑,有重大upregulation Nrf2的一小部分脑细胞存活。
”,告诉你,这些细胞能够使高水平的Nrf2可以生存,”托马斯说。他们不知道至少在帕金森症的一部分问题是,高水平的Bach1防止Nrf2通路被激活。有趣的是,他们也有证据表明,它可能不需要太多Nrf2将更多的细胞变成幸存者。至少在动物模型和人类细胞在文化、Nrf2水平不显著改变Bach1基因删除但表达的抗氧化基因下游肯定做的。
”,告诉你,也许我们不需要很多Nrf2表达,也许只是一个基底数量就够了,”托马斯说。
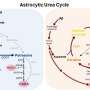
Nrf2通路活性随年龄的增长会慢慢下降,其下降加速在帕金森氏症,不仅帮助控制随意运动产生多巴胺的神经细胞,但也在星形胶质细胞,另一个大脑细胞类型有助于滋养和保护他们。其他人显示upregulation Nrf2仅在星形胶质细胞,阻止神经元死亡。
“科学家已经证明,如果你人为Nrf2在星形胶质细胞过表达,可以防止多巴胺能神经元死亡。我们问同样的问题:你能保护多巴胺神经元如果你抑制星形胶质细胞Bach1 ?”Thomas says.
Bach1抑制显示潜在的受益范围广泛的问题,从脊髓损伤、动脉粥样硬化和脑感染但托马斯是最早探索帕金森的潜力。他之前的工作由迈克尔·j·福克斯基金会帮助建立Bach1作为一个潜在的目标。
而激活Nrf2是科学家,不是一个新目标领域主要试图通过干扰与Keap1的关系。但迄今为止,这些疗法改变了Keap1参与许多蛋白质在细胞中需要的地方,并不时采取一些垃圾。
“当Keap1功能改变,需要你牺牲其他蛋白质从细胞被删除,导致毒性物质在细胞中它会死,”他说。“我们是压倒一切的这Keap1 / Nrf2途径。”But he notes that he is among those still pursuing ways to disrupt the Keap1/Nrf2 connection without harming Keap1.
托马斯还指出,我们活跃的固有财产产生多巴胺的神经细胞自发产生氧化的氧,导致本已高氧化负载,使这些脑细胞特别脆弱。
大约10%的帕金森运行在家庭。大多数情况下很可能由于环境因素,如农药接触,和遗传学。老化是一个主要的风险因素。
托马斯和他的同事们报告《神经科学杂志》上2016年6月的代谢物药物用于治疗多发性硬化症Nrf2更直接的目标,减少潜在的副作用,如腹泻、恶心、呕吐和大脑父药物引起的感染。dimethylfumarate,父药物及其代谢物,monomethylfumarate,明显减缓的损失中产生多巴胺的神经元在大脑中。
进一步探索