新的阿尔茨海默氏症动物模型更接近于模拟人类疾病
宾夕法尼亚大学佩雷尔曼医学院的研究人员通过将人类阿尔茨海默病大脑病理tau蛋白提取物(来自死后捐赠的组织)注射到大脑中含有不同数量的淀粉样蛋白β (Aβ)斑块的小鼠中,发现淀粉样蛋白β促进了斑块和异常tau蛋白之间的相互作用。这种关系促进了神经元中突变tau蛋白的传播,这是长期阿尔茨海默病的标志。他们本周在《科学》杂志上发表了他们的发现自然医学.
宾夕法尼亚大学神经退行性疾病研究中心(CNDR)主任、资深作者Virginia M-Y Lee博士说:“在与AD更相关的背景下,制作一种包含a β和tau病理的AD小鼠模型一直很受欢迎,但很难完成。”“这项研究是阿尔茨海默症研究的一大步,它将使我们能够在更现实的背景下测试新的疗法。”
阿尔茨海默病的特征是细胞外的Aβ斑块和细胞内的tau团块。研究人员提出,Aβ斑块是AD的起始病理,但所有基于去除Aβ的AD临床试验的失败挑战了这一假设和仅针对Aβ治疗AD的想法。与此同时,来自其他研究的证据,包括CNDR的研究,强烈地将tau团块的扩散与AD认知能力的恶化联系起来,但这两种病理之间的确切联系仍然是谜。
Tau蛋白在稳定轴突中的微管方面起着类似铁路轨道交叉的作用,轴突负责在神经元内运输物质。由于tau蛋白在神经细胞中聚集,从微管中去除会导致受影响的神经元功能失调,最终导致它们死亡和AD。
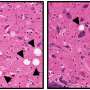
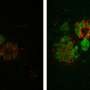
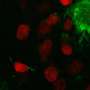
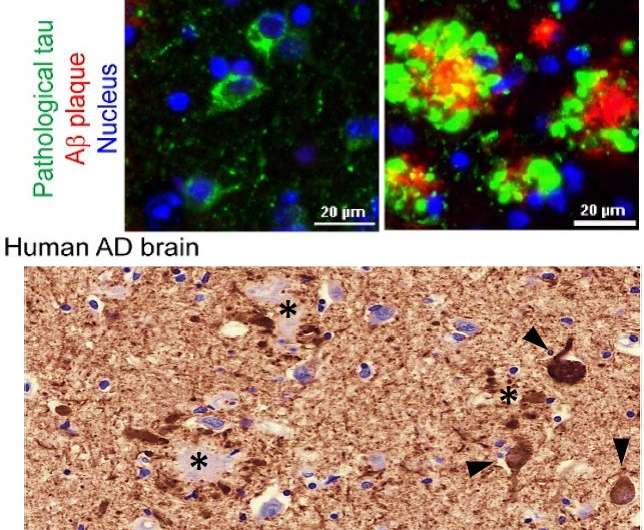
宾夕法尼亚大学的研究小组在他们的新小鼠模型中模拟了三种主要类型的ad相关tau病理的形成:神经原纤维缠结、神经线和围绕Aβ斑块的tau聚集物,称为神经神经性斑块τ。“这是我们第一次在小鼠模型中看到并研究a β斑块周围的营养不良轴突中的tau团块,就像我们在患有AD的人脑中看到的一样,”第一作者何卓浩博士说,他是Lee实验室的博士后。
研究小组发现,Aβ斑块创造了一种环境,促进病理性tau快速扩增和扩散成大聚集物,最初表现为神经斑块tau。随后,神经纤维缠结和神经线向其他神经元形成和扩散。这些tau蛋白的形成也损害了小鼠的大脑功能,包括记忆障碍。
这项研究是解释a β斑块环境如何加速tau病理在AD患者大脑中的扩散的新方法的基础,这与对死后AD大脑的成像研究和调查一致。
这些发现为治疗AD患者提供了新的靶点和策略。“我们的新小鼠模型现在可以用来测试针对一种或两种病理的治疗方法,看看是联合治疗还是单靶点治疗更好,”李说。