胶质母细胞瘤生存机制揭示新的治疗靶点
西北医学的一项研究,发表在杂志上癌症细胞,为胶质母细胞瘤肿瘤生存机制提供了新的见解,并证明抑制这一过程可以增强放射治疗的效果。
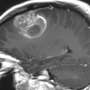
胶质母细胞瘤是最常见和最具侵袭性的脑肿瘤类型,预后特别差。患者接受手术治疗,放射治疗还有化疗,但无法治愈。
先前的研究表明,自噬——细胞破坏的自然过程,在应激条件下也起保护作用——有助于肿瘤的生存和生长,并由常见的癌症治疗诱导,使肿瘤对治疗产生耐药性。因此,人们对抑制这种生存机制非常感兴趣。
在目前的研究中,科学家试图了解调节癌症自噬的分子机制,这可能为未来的治疗揭示新的靶点。
“我们的发现巩固了自噬在恶性肿瘤中促进作用的概念胶质母细胞瘤,并指出了针对胶质母细胞瘤和其他肿瘤的特异性自噬与一线治疗(如放疗)相结合的必要性,”首席研究员Shi-Yuan Cheng博士说,他是神经肿瘤学部门的神经病学教授,也是西北医学Lou and Jean Malnati脑肿瘤研究所和西北大学Robert H. Lurie综合癌症中心的成员。
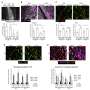
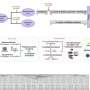
在这项研究中,科学家们首先确定了一种名为MST4的蛋白激酶在胶质母细胞瘤中起着促进肿瘤的作用。然后,他们第一次确定了MST4的底物,称为ATG4B,它通过增加自噬活性来介导MST4的肿瘤促进作用。
研究小组进一步证明,辐射诱导MST4表达和ATG4B磷酸化,从而促进有助于肿瘤生存的自噬过程。
最后,科学家们研究了ATG4B抑制剂在脑胶质母细胞瘤原位异种移植模型中的作用。他们表明,当与放疗联合使用时,该抑制剂显著减缓了肿瘤生长,提高了荷瘤动物的总体存活率。
“我们在胶质母细胞瘤中发现了一个促自噬信号轴,其药理学抑制增强了抗肿瘤Cheng解释说,并指出这些发现有可能转化为临床治疗。
程还是另一项研究的合著者,发表在自然通讯该研究在11月发现了一种名为TRIM24的蛋白质,它是由表皮生长因子受体(EGFR)基因突变驱动的胶质母细胞瘤的转录共激活因子。这篇论文表明TRIM24可能是这类癌症的潜在治疗靶点。