基因治疗恢复患有1型糖尿病的小鼠血糖水平
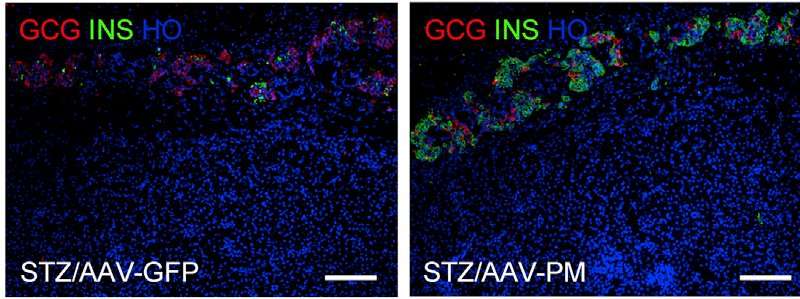
1型糖尿病是一种慢性疾病,其中免疫系统攻击并破坏胰腺中的胰岛素产生的β细胞,导致血糖的高血液水平。1月4日出版的一项研究细胞干细胞证明了基因治疗方法可以导致功能性β细胞的长期存活以及糖尿病小鼠延长时间的常规血糖水平。研究人员使用腺相关病毒(AAV)载体向小鼠胰腺两种蛋白质,PDX1和MAFA递送,该α细胞重新编程为功能性,胰岛素的β细胞。
“这项研究基本上是对临床可转译的、简单的自身免疫单一干预的首次描述糖尿病匹兹堡大学医学院的资深研究作者George Gittes说:“这将导致正常的血糖,而且重要的是没有免疫抑制。”“考虑到糖尿病逆转的令人印象深刻的本质,以及对患者进行AAV基因治疗的可行性,在不久的将来对1型和2型糖尿病患者进行临床试验是相当现实的。”
世界上大约9%的成年人口有糖尿病,这可能导致心脏病,神经损伤,眼问题和肾病等严重的健康问题。糖尿病治疗的一个基本目标是保留和恢复功能性β细胞,从而补充称为胰岛素的激素水平,其将血糖移动到细胞中以促进其能量需求。但在1型糖尿病患者中,β-细胞替代疗法可能注定失败,因为新细胞可能会使受害者成为摧毁原始细胞的同样的自身免疫。
对该问题的潜在解决方案是将其他细胞类型重新编程为功能β样细胞,其可以产生胰岛素,但与β细胞不同,因此不受免疫系统识别或攻击。为了探讨这种方法的可行性,Gittes和第一个作者匹兹堡大学医学院的Xiangwei Xiao工程化了AAV载体,递送到称为PDX1和MAFA的小鼠胰腺蛋白,其支持β细胞成熟,增殖和功能。目标是从胰腺产生功能β样细胞α细胞,这可能是β电池更换的理想源。例如,α细胞是丰富的,类似的β细胞,并且在正确的位置,所有这些都可以促进重编程。
通过比较正常的基因表达模式β细胞和胰岛素产生源自α细胞的细胞,研究人员已经证实了几乎完全的细胞重编程。该基因治疗方法恢复正常血糖水平在糖尿病小鼠延长一段时间,通常约为四个月,并且新的胰岛素产生的细胞几乎完全来自α细胞。此外,该策略成功地产生了来自人α细胞的功能性胰岛素的细胞。
“病毒基因治疗似乎产生了对自身免疫攻击相对抗性的新胰岛素产生的细胞,”Gittes说。“这种阻力似乎是由于这些新细胞与正常胰岛素略有不同细胞,但没有那么不同,他们不起作用。“
这种方法的几个特征可以促进对人类的翻译。对于一种,作为本研究中使用的AAV载体目前正在进行人类中的各种基因治疗试验。此外,病毒载体可以通过常规进行的非手术内窥镜程序直接递送到人胰腺中;但是,该程序可以引发胰腺炎。此外,不需要免疫抑制,因此患者将避免相关的副作用,例如感染风险增加。
然而,一个主要问题是小鼠最终恢复到糖尿病状态,这表明这种治疗不会代表这种疾病的明确治愈。虽然有些研究表明,小鼠在小鼠中的反复性糖尿病的保护并不是永久性的,但小鼠的过程高度加速,因此小鼠中的四个月可能会翻译到人类的几年内,“格蒂斯说。
目前,研究人员正在灵长类动物身上测试他们的方法。“如果我们能够在非人类灵长类动物身上显示出有效性,我们将开始与FDA合作,以获得使用这种病毒的批准基因治疗在1型和2型糖尿病患者中,”Gittes说。
进一步探索











用户评论