科学家发现了调节肌肉和心脏功能所需蛋白质的关键机制

Centro Nacional De Investigaciones Cardiovashulares Carlos III(CNIC)和哥伦比亚大学在纽约哥伦比亚大学发现了一种在调节骨骼肌和心脏功能中起重要作用的重要机制。今天发表的研究自然通信并由CNIC研究员Jorge Alegre-Cebollada协调,描述了调节巨蛋白三蛋白的弹性的新机制。Aline-Segre-Cebollada解释的是一个关键的蛋白质,在整个身体的横纹肌肉作用中,特别是在心脏:“这证明是三肽基因中的突变是影响身体肌肉的疾病的常见原因和心脏。“
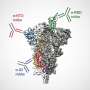
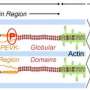
Titin是最大的蛋白质在人体内有多种功能。根据豪尔赫·阿莱格-塞波拉达的说法,“简单地说,我们可以把肌凝素看作是一个‘分子弹簧’,它允许肌肉细胞同步收缩。”然而,它不是一个简单的弹簧,决定肌动蛋白弹性的许多机制包括其结构中称为免疫球蛋白域的特定区域的展开。总之,肌凝蛋白的弹性是由蛋白内100多个免疫球蛋白结构域的协同作用决定的。
利用生物信息学和结构生物学方法,研究团队发现免疫球蛋白结构域具有较高的半胱氨酸含量。这种氨基酸具有特殊的性质。Jorge Alegre-Cebollada解释说:“当蛋白质中的两个细胞素靠近彼此时,它们可以在多肽链的不同部分之间形成一种化学连接,称为二硫键。”研究人员观察到,肌凝素中的许多免疫球蛋白结构域形成二硫键,参与其中的半胱氨酸可以动态变化,这一过程称为异构化。“最有趣的发现是二硫键引起了肌锡弹性性能的重大变化"
二硫键的形成是被称为还原-氧化(redox)的更广泛的生化转化的一个例子。人们早就知道,许多疾病的过程影响心,包括心肌梗死,包括心肌的氧化还原状态的突然和剧烈的变化。
Alegre-Cebollada博士目前正在调查我们的细胞如何修改titin.氧化还原状态是调节骨骼和心脏的一种机制肌肉活性和不同的疾病如何干扰蛋白质的机械作用,导致功能的丧失。alegrea - cebollada总结道:“我们的机械发现是通过在体外重组收缩系统而成为可能的。虽然我们已经通过这种方法学到了很多,但现在的挑战是了解这些基本原理是如何在生物体中运作的。这是我们目前研究的重点,采用多学科的方法,结合了生理学、生物学和生物化学的先进技术。”
该研究是Alegre-Cebollada博士与哥伦比亚大学朱廖福尼亚教授之间合作的结果。Fernández教授是开发单分子生物物理技术的先驱,用于研究蛋白质的机械性能,他与Alegre-Cebollada博士的合作使得可以描述蛋白质力学的生化调控。
进一步探索











用户评论