研究人员找到了一种“挨饿”癌症的方法
范德比尔特大学医学中心(VUMC)的研究人员首次证明,有可能饿死肿瘤并通过新发现的小型化合物来阻止其摄取至关重要的营养谷氨酰胺。
他们的发现,本周报道自然医学,为开发潜在的“范式转移”疗法的基础奠定基础癌症细胞代谢可以通过正电子发射断层扫描(PET)成像进行非侵入性监测。
范德比尔特分子探针中心的科学主任,本文的相应作者科学主任查尔斯·曼宁(Charles Manning)说:“癌细胞表现出独特的代谢需求,可以在生物学上与其他健康细胞区分开。”“癌细胞的代谢特异性为我们提供了丰富的化学,放射化学和分子成像,以发现新的癌症诊断和潜在疗法。”
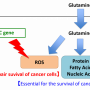
谷氨酰胺是许多细胞功能的必需氨基酸,包括生物合成,细胞信号传导和保护氧化损伤。因为癌细胞比正常细胞更快地分裂,所以它们需要更多谷氨酰胺。
一种称为ACST2的蛋白质是谷氨酰胺的主要转运蛋白到癌细胞中。升高的ASCT2水平与许多人类癌症(包括肺,乳腺癌和结肠)的生存率差有关。沉默癌症ACST2基因的遗传研究细胞已经产生了戏剧性的抗瘤效果。
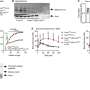
范德比尔特的研究人员进一步走了一步:他们开发了V-9302,这是谷氨酰胺转运蛋白的第一个高功能的小分子抑制剂。在癌细胞在体外和小鼠模型中生长的ACST2的药理学阻断,V-9302导致降低癌细胞生长和增殖,氧化损伤增加和细胞死亡增加。
定位谷氨酰胺代谢研究人员总结说,在转运蛋白水平上,代表了“精确癌症医学中的潜在可行方法”。
然而,“将患者与谷氨酰胺依赖性肿瘤和这种新型抑制剂配对将需要经过验证的生物标志物”。这是因为对V-9302的反应更多地取决于ACST2转运蛋白的活性,而不是转运蛋白基因的表达。
幸运的是,与正常的周围组织相比,可以开发创新的宠物示踪剂来检测肿瘤的谷氨酰胺代谢率的增加。
目前,VUMC正在进行五项临床试验,以测试一个名为18F-FSPG的新宠物示踪剂的诊断潜力,以可视化肺,肝,卵巢和结肠的肿瘤。曼宁(Manning)和他的CMP同事还将包括11C谷氨酰胺在内的其他谷氨酰胺代谢示踪剂带入了范德比尔特(Vanderbilt)的临床试验。
通过将成像同位素连接到V-9302,曼宁的组还可以查看该化合物是否达到其靶标 - 谷氨酰胺代谢率高的肿瘤。
曼宁说:“如果我们可以根据某种药物来帮助我们预测哪种肿瘤会积累该药物,因此在临床上容易受到伤害,这是本质上的本质“可视化”精密癌症医学。
范德比尔特 - 伊格兰癌症中心正在资助曼宁所说的这种“治疗方法”的发展 - 治疗和诊断的结合。
进一步探索