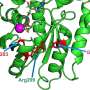
“诱导多能性”细胞衍生内耳细胞可能改善先天性听力损失
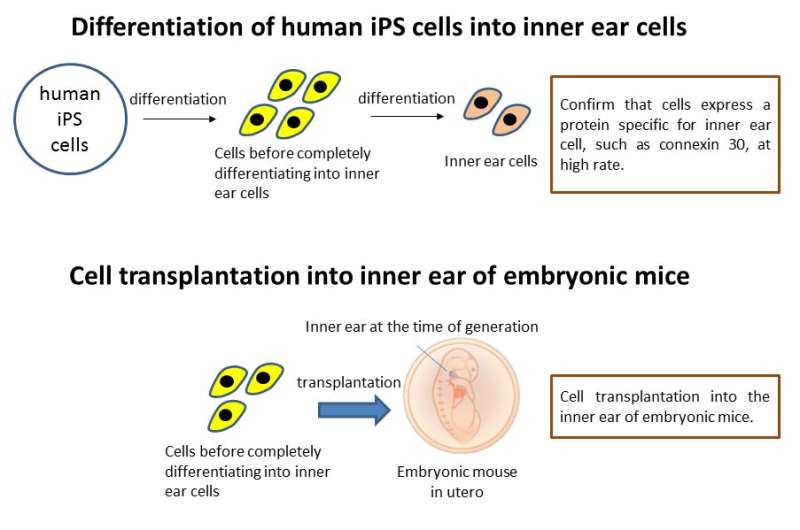
日本研究小组已经成功移植人类“诱导多能性”细胞衍生内耳细胞表达来自人体的蛋白质胚胎内耳的老鼠。遗传性听力损失约占一半的先天性听力损失情况下,这工作是一个主要的贡献对研究目标的胚胎内耳。
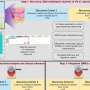
入射频率的一个每500 - 1000新生儿先天性听力损失是最常发生的先天性疾病,和大约一半的先天性听力损失情况下是世袭的。治疗这种听力损失包括耳蜗植入和助听器,但没有根本的治疗。
在人类遗传性听力损失,耳聋已经发生在胎儿发育,所以治疗在这个阶段是最有效的。GJB6基因编码联接蛋白30蛋白质,在听力的发展至关重要,缺乏基因的结果中第二常见的疾病情况下的遗传性听力损失在内耳,没有其他疾病。
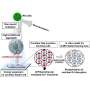
在以往的研究中,博士Ryosei Minoda,熊本总医院耳鼻咽喉部主管,报道称,恢复了听力损失的内耳基因治疗联接蛋白30-deficient胎儿老鼠。当前的研究小组,其中包括Minoda博士和Hiroki熊本大学的武田和几个庆应义塾大学的研究人员,已经成功移植人类ips的衍生细胞胚胎内耳的老鼠,一个壮举与高水平的技术困难。
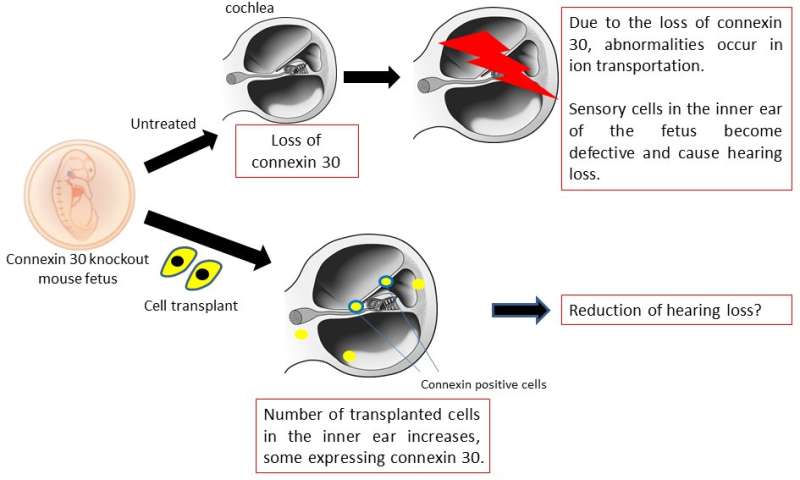
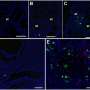
首先,研究小组成功地有效地诱导内耳内耳细胞表达特定的蛋白质,如联接蛋白26日联接蛋白30日和Pendrin,从人类的“诱导多能性”细胞。他们将内耳细胞的祖细胞移植到胚胎正常的内耳和联接蛋白30基因敲除小鼠用玻璃管尖尺寸进行了优化。移植的细胞移植到各种网站在两组的内耳。然而,联接蛋白30基因敲除小鼠比正常小鼠移植细胞,和一些移植细胞表达联接蛋白被发现30。
这一事实联接蛋白30基因敲除小鼠移植细胞的数量高于正常老鼠,一些移植细胞表达联接蛋白30是一个非常重要的发现当考虑细胞移植作为治疗遗传性听力损失由接合素不足造成的。细胞移植可以弥补缺失的联接蛋白,可以提高听力损失通过添加运转正常联接蛋白的蛋白质。未来的工作将试图提高移植细胞的数量,提高听力能力。预防听力损失是一个令人兴奋的前景。
此外,这项研究表明细胞来源于人类可以移植到小鼠胚胎的杂合的内耳。这增加了体内实验的可能性,使用来自人体的老鼠胚胎细胞治疗效果。人们认为,这一研究可以大大有助于遗传的基本治疗的发展听力损失和内耳的开发研究。
进一步探索