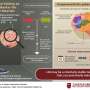
天花疫苗研究产生有利的结果
巴伐利亚北欧的官员昨日宣布成功的3期临床试验的结果由USAMRIID证明公司的安全性和有效性的临床实验,IMVAMUNE non-replicating天花疫苗。
产品正在开发替代当前美国的许可复制天花疫苗,ACAM2000,不能使用特定的人群,包括过敏性皮炎和艾滋病患者。它已经批准了在加拿大和欧盟。
USAMRIID研究总监菲利普·r·皮特曼,医学博士与美国国防卫生机构合作,招收440名受试者在美军在韩国。随机、非盲的研究有两个co-primary端点。第一个是显示IMVAMUNE诱导非劣抗体反应与ACAM2000相比。在这项研究中,峰值中和抗体引起IMVAMUNE被证明是双重的高于刺激ACAM2000,展示一个统计上优越的免疫反应。
第二个co-primary端点是展示一个“花”的衰减或预防与IMVAMUNE志愿者之前接种疫苗。从历史上看,将是一个衡量有效性的第一次对天花接种疫苗的人。它由一个脓包,痂和皮肤上的疤痕,发达后初始接种天花疫苗,如ACAM2000复制。第二次接种后,那些已经开发了一种保护免疫反应显示一个减少或没有。这也是实现USAMRIID-Bavarian北欧研究。
“如果得到批准,这个疫苗将会直接影响改善力健康保护美国士兵和其他服务成员需要打疫苗吗天花上校说:“加里•惠勒USAMRIID的司令。
根据保罗·卓别林,总裁兼首席执行官巴伐利亚的北欧,IMVAMUNE已经给超过7800名受试者在21个临床研究,包括这个试验和另一个第三阶段的研究。他说,公司计划文件生物许可应用程序与美国食品和药物管理局今年晚些时候。
“这个项目才可能通过无数的一致和大力支持美国政府机构和展示了可以通过一个成功的公私合作伙伴关系来保护公众的故意释放天花病毒,”卓别林说。
更多信息:研究可查看详情clinicaltrials.gov / ct2 /显示/ NCT01913353