交通堵塞导致免疫细胞路怒症
OCRL基因突变导致劳综合征但目前尚不清楚OCRL的缺失如何导致患者遭受不同的眼睛、肾脏和神经系统症状。在十月号的专题文章中公共科学图书馆遗传学我们报告说,果蝇中OCRL的缺失会导致免疫细胞的不适当激活,这提高了炎症可能是某些Lowe综合征症状的原因的令人兴奋的可能性。
苍蝇为罗氏综合症提供了新的见解
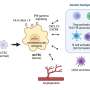
OCRL基因编码一种酶,这种酶控制着细胞中多种类型脂质膜的组成。这是理解洛的一大挑战并发症状一直以来,OCRL似乎在细胞中扮演着几种不同的角色,包括控制它们如何分裂,如何感知周围环境,以及如何在称为核内体的细胞内隔室中存储和运输物质。大多数研究OCRL的实验都是在培养细胞上进行的,我们推断,测试OCRL在完整生物体中的工作位置和方式可能有助于梳理出其最相关的功能。为此,我们删除了果蝇的OCRL同源体,意外地发现突变体表现出巨噬细胞样的激活免疫细胞.这些细胞有许多在缺乏OCRL的培养细胞中观察到的相同问题,包括细胞分裂、内吞作用和内体转运的缺陷。有趣的是,我们发现无论是细胞分裂缺陷还是内吞作用缺陷都不能解释免疫细胞表型,这表明内体运输存在问题。
交通堵塞会激活免疫细胞
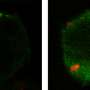
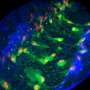
内体运输控制摄取,分类,回收和降解的信号范围广泛,调节各种细胞行为。这个过程是高度动态的,正如十月号的封面图片所示公共科学图书馆遗传学(另见电影在这里)。这些运输动态依赖于一个称为Rabs的蛋白质家族,它决定了不同类型的核内体的功能,并控制它们之间货物的移动。
为了测试核内体运输是否参与到OCRL突变表型中,我们在基因上操纵了免疫细胞中Rab蛋白的活性。我们发现了Rab7和Rab11的主要作用,这两种Rabs有助于在回收和降解的核内体之间进行货物分类。在其他正常的免疫细胞中,Rab7的激活或Rab11的失活导致了类似于OCRL缺失的表型。此外,对每个Rab的相反操作都能够抑制OCRL突变体中的免疫细胞激活,这表明这一分选步骤是OCRL在免疫中的关键作用位点细胞.展望未来,确定这种交通变化如何影响特定的免疫相关信号将是至关重要的。
劳氏综合征患者癫痫发作的潜在联系?
一些证据表明,我们观察到的免疫细胞激活与洛氏综合征患者的癫痫发作有关。我们发现,OCRL突变体放大了调节人类大脑炎症反应的多种免疫信号,包括toll样受体和IL6。重要的是,这些炎症通路与人类癫痫发作障碍有关。其他研究小组已经确定了OCRL与炎症之间的直接联系:斑马鱼中OCRL的缺失会导致大脑中的囊性病变和癫痫易感性,而癫痫小鼠模型中的癫痫诱导会改变大脑星形胶质细胞中的OCRL水平[3,4]。总之,这些数据表明炎症可能是一种很有前途的研究Lowe综合征患者癫痫症状的新途径。
进一步探索
癫痫的实验研究:免疫和炎症机制。Semin儿科神经科.2014; 21(3): 197 - 206。Epub 2014/12/17。pmid: 25510941
Ramirez IB, Pietka G, Jones DR, Divecha N, Alia A, Baraban SC,等。罗氏综合征斑马鱼模型神经发育受损。哼Mol Genet.2012; 21(8): 1744 - 59。Epub 2012/01/03。pmid: 22210625
张娟,张建平,张建平,等。匹罗卡品颞叶癫痫模型中急性和慢性反应性星形胶质细胞的分子分析。一般人说.2016; 91:315-25。Epub 2016/04/10。pmid: 27060558
本文转载自PLOS博客:blogs.plos.org.