药物治疗稀有结核硬化复合体批准的皮肤病变
大阪大学的科学家开发了一种新药治疗肿块硬化症复合体(TSC),是一个罕见的顽固性疾病,是一个世界第一。在由大阪大学的医生主导的临床研究I和II后,药物公司的III期临床试验,该药物在索格克斯指定系统的6个月内批准,由日本政府领导的早期批准系统,2018年3月23日,然后被商业化。
该药物是由Sakigake系统指定的第一药。医师导向的临床研究I和II的细节已发表于此JAMA皮肤科2017年1月。
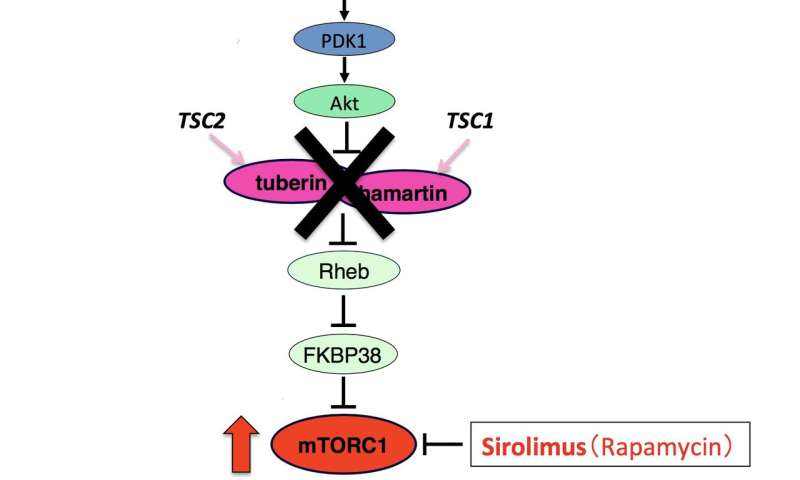
TSC是一种遗传的常染色体显性疾病由TSC1(Hamartin)和TSC2(Tuberin)基因突变引起的。TSC1和TSC2肿瘤抑制基因中的突变导致MTORC1(哺乳动物催盲素综合体1)的突变激活,在众多器官中发育叫做Hamartoma的肿瘤病变,例如大脑,皮肤,肾脏和肺部。
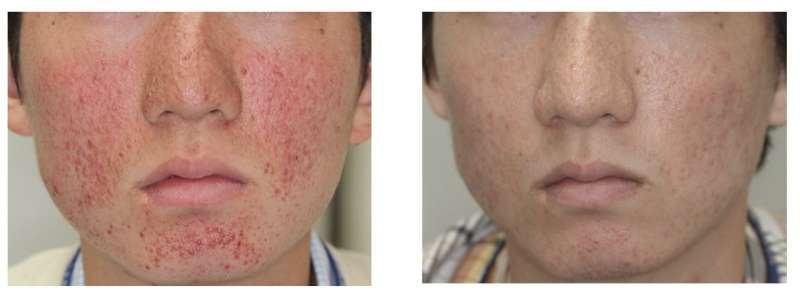
TSC的症状包括癫痫,学习障碍,发展延误和自闭症谱系障碍除了是海马拉姆。各种症状,皮肤问题,如面部血管纤维瘤,超过90%的TSC患者发展。出血,继发细菌感染与病变相关的疼痛和功能性紊乱造成患者的痛苦,严重影响了他们的美容原因的生活质量。然而,目前,已建立的治疗剂仅限于手术疗法,这些疗法难以在没有全身麻醉的情况下对小孩和智障患者进行智障患者。
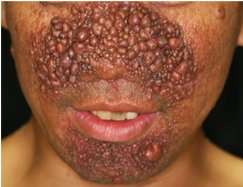
西罗莫司(雷帕霉素)的全身施用减少了肿瘤体积,减少了TSC中肿瘤的发红;然而,全身治疗可能导致不利影响。因此,由Mari Wataya-Kaneda领导的研究组进行了MTORC1抑制剂的局部凝胶作为更安全的治疗剂的研究和开发,考虑了局部西罗莫司制剂,以增强具有大分子量的有效成分的吸收。
该局部西罗莫猴凝胶是唯一可以在TSC中局部施用于皮肤病变的唯一药物。批准这种无痛,安全,易于使用的药物,可以安全有效地治疗皮损在TSC中。此外,Sakigake制度和行业 - 政府大学合作在批准方面非常好药品,这将有助于在未来制定治疗其他难治性疾病的药物。
进一步探索













用户评论