研究报告可能的新方法,以停止不可治疗的小儿脑癌
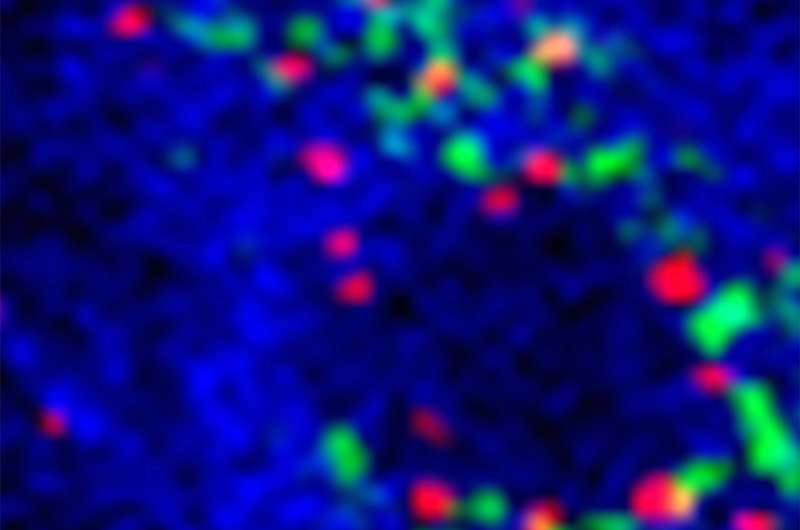
研究人员在临床前实验室测试中使用了一种实验性分子疗法,有效地治疗了几种类型的致命儿童脑癌,现在他们提议将这种疗法推进到儿童的临床测试中。
辛辛那提儿童癌症和血液疾病研究所的科学家在该杂志上发表了报告分子癌症治疗测试小分子6-硫代-2'脱氧鸟苷(6-硫代- dg)大脑癌症干细胞来源于病人捐献的肿瘤细胞。研究人员还在儿童脑癌的人格化小鼠模型上测试了这种治疗方法。
这些癌症包括固有脑桥胶质瘤(DIPG)、高级别胶质瘤(HGG)和高危成神经管细胞瘤(MB)。
在临床前的实验室测试中,靶向分子疗法在小鼠模型中通过了身体的保护性血脑屏障——导致癌细胞的广泛DNA损伤,并阻止或减缓了两种无法治愈的儿童脑癌。科学家们说,这种疗法不会影响动物体内的非癌细胞。治疗结束后,6-硫代dg的治疗效果在动物中继续。
“这些发现表明,6-硫代dg是一种有前途的治疗耐药性的新方法小儿脑瘤他们为在患有脑瘤的儿童中进行这种治疗的临床试验提供了理论依据,”肿瘤科高级研究研究员Rachid Drissi博士说。
需要更多的研究
尽管6-硫代dg似乎不会进入非癌细胞,但Drissi强调,在对患者进行临床试验之前,还需要进行更多的研究以确保化合物的安全性。这些研究正在进行中。
尽管经过几十年的研究和技术进步,DIPG和其他高危儿童脑癌仍然没有得到有效的治疗。
该研究表明,注射后,6-硫代dg首先通过DIPG小鼠模型的血脑屏障发挥作用,这是一个重大进展,消除了药物治疗脑癌的主要障碍。的血脑屏障保护器官免受病原体通过循环系统,使其药理学上无法穿透。
打断不朽
这种化合物的作用原理是在脑癌细胞中引发广泛的DNA损伤癌症干细胞。研究人员称,为了达到这一目的,这种化合物会破坏脑癌细胞染色体端粒的功能。
端粒是染色体末端重复的DNA序列,可以防止或减少细胞内的遗传不稳定性。随着细胞衰老,端粒通常会缩短,而遗传的不稳定性有助于杀死衰老细胞。但脑癌细胞之所以能永生,是因为它们的端粒长度继续由端粒酶维持,这使得细胞难以或不可能被杀死。
Drissi和他的同事在早期的研究中发现,73%的DIPG肿瘤和50%的高级别胶质瘤具有端粒酶。从本质上说,端粒酶有助于癌症细胞保持端粒的长度。
这使得研究团队使用了6-硫代dg的治疗方案,该方案已经在另一家机构的肺癌临床前研究中进行了测试。化合物6-硫代dg被制造成类似于端粒中自然产生的成分。注射并进入大脑后,6-硫代dg被纳入癌症细胞染色体,导致端粒酶依赖端粒损害。
进一步探索














用户评论