PARP-1可能是PARP抑制剂有效性的关键,现在研究人员可以成像它
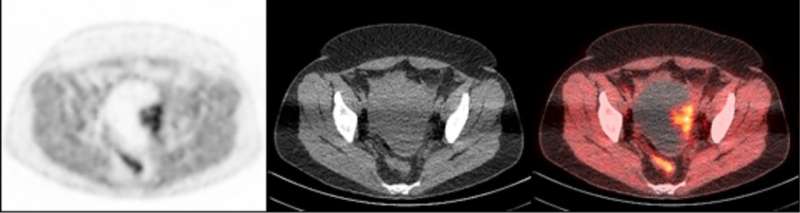
宾夕法尼亚大学医学院的研究人员使用CRISPR/Cas9基因编辑技术分离出了一个可能导致卵巢癌患者对PARP抑制剂产生耐药性的关键遗传特征,他们也证明了他们有一种使用PET成像来观察该特征的方法。
研究小组发现了PARP抑制剂——一种致命的靶向疗法癌症DNA突变的细胞修复基因,同时保留没有突变的健康组织——特别需要PARP-1的存在才能生效。他们还表明,宾夕法尼亚大学开发的一种放射性示踪剂使PARP-1在PET扫描时可见,并可能提供一种测量PARP-1的方法卵巢癌这是对活检的补充。来自宾夕法尼亚大学佩雷尔曼医学院的放射学家、病理学家和肿瘤学家组成了这个多学科团队,他们的研究成果发表在《美国医学杂志》上临床调查杂志本月。
上皮性卵巢癌是女性第五致命的癌症类型,超过70%的患者在被诊断时已经表现出疾病的晚期。标准的治疗依赖于化疗,但最近,PARP抑制剂已成为改善患者预后的一种方法。其中三种药物目前已被美国食品和药物管理局批准使用,如果患者的基因突变BRCA1和BRCA2检测呈阳性,通常会接受这些抑制剂。然而,只有大约50%的患者有反应。
宾夕法尼亚大学的研究人员使用CRISPR/Cas9基因编辑在实验室中删除PARP-1卵巢癌细胞然后将这些细胞暴露于PARP抑制剂中,并将它们与含有PARP-1的对照组进行比较。与未编辑的对照组细胞相比,没有PARP-1的细胞显示出较少的DNA损伤和较少的抑制反应。在一个案例中,PARP-1的缺失导致对PARP抑制剂的敏感性下降超过1000倍。
“这些发现表明PARP抑制剂发挥作用需要PARP-1,”该研究的共同资深作者、药学博士、RPh、BCNP、放射学讲师Mehran Makvandi说。“这些数据还表明,临床需要评估BRCA癌症中的PARP-1水平,以更好地了解哪些患者可能受益,哪些可能耐药。”
为了达到这个目的,研究人员使用了一种放射性示踪剂与PARP-1结合,使其在PET扫描时可见。这种示踪剂被称为FluorThanatrace,是由放射学布里顿·钱斯教授罗伯特·h·马赫博士特别设计的。在使用小鼠模型进行的临床前试验显示示踪剂击中了其特定的分子靶标后,该研究的作者进入了第一阶段试验。
一项涉及10名患者的临床试验获得了13个组织样本。这些样品对示踪剂的吸收具有广泛的光谱,但这种吸收与PARP-1的表达相关。换句话说,示踪剂与肿瘤结合越多,肿瘤表达的PARP-1水平就越高。
Makvandi说:“这是一个概念证明,我们不仅有PARP抑制剂有效性的潜在生物标志物,而且我们还拥有一种非侵入性成像技术,可以在卵巢癌患者中找到这种生物标志物。”
研究人员表示,这项工作的下一步是评估这项技术是否可以用来预测PARP抑制剂的疗效和耐药性。Makvandi和Fiona Simpkins,医学博士,产科和妇科助理教授和这项研究的合著者,正在领导未来的临床试验,直接测试这种方法对卵巢癌的预测价值病人接受PARP抑制剂单一疗法。乳腺癌的试验也在计划之中。
进一步探索






用户评论