双管齐下的方法可以抑制许多肺癌病例
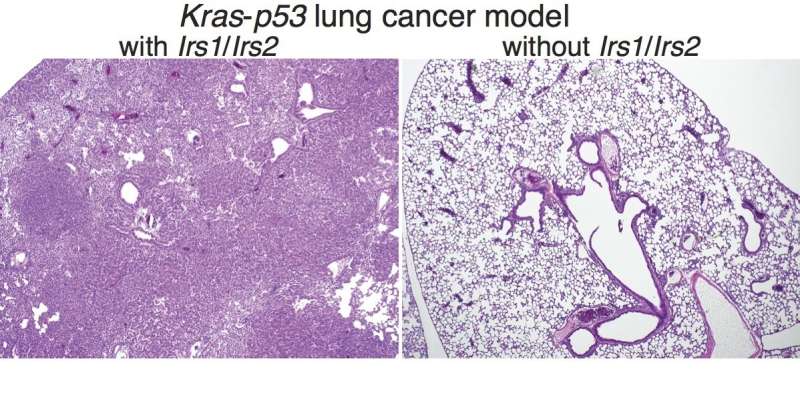
非小细胞肺癌,最常见的一种肺癌是癌症死亡的主要原因在美国一项新的研究表明,大约在4例,那些由喀斯特致癌基因,可成功治疗临床药物的组合已经可用。波士顿儿童医院的研究今天发表在国家科学院的诉讼程序(PNAS)。
30多年来,科学家们一直试图用药物靶向KRAS突变致癌基因,但收效甚微。因此,一些研究人员试图以相关的生物途径为目标。
其中一个途径涉及胰岛素和胰岛素样生长因子-1 (IGF-1),它们影响营养物质的摄取和释放,并最终影响细胞的生长。但这一途径还没有被明确证明是kras驱动的燃料肺临床试验到目前为止,IGF-1信号传导的癌症和抑制剂已经失败。实际上,最近的小鼠研究其实看到肺肿瘤变得更加激进。然而,这项研究仅部分地靶向胰岛素/ IGF-1信号。
在新的研究中,研究人员使用遗传技术来完全阻断胰岛素/ IGF-1信号,提供最佳测试场,用于研究途径在KRAS驱动中的作用肺癌。该模型证实了完全阻断该途径可以减缓肿瘤生长,但也证明了需要第二步来完全抑制它。
“我们的研究使用了一种强有力的方法来阻断胰岛素/IGF-1信号,并解决了kras突变肺中的一个长期存在的问题癌症波士顿儿童医院内分泌科的研究员、论文的资深作者Nada Kalaany博士说。“当你使用遗传学时,结果会更有说服力。”
一种新的肺癌生长因素效果的新模型
Kalaany的团队通过穿过两种小鼠的菌株创造了新模型:一种良好的菌株,模拟KRAS驱动的肺癌,以及缺乏胰岛素/ IGF-1信号传导的另一种菌株,以前由Morris White,Ph.D。波士顿孩子们要研究糖尿病。该第二模型删除了两个键基因,称为IRS1和IRS2,其编码所谓的“适配器”蛋白质,该蛋白质是胰岛素/ IGF-1信号传导所必需的(20世纪80年代的白色发现)。
新的交叉繁殖小鼠提供了最佳模型,用于研究肺癌中的胰岛素/ IGF-1信号。研究人员继续表明,当在肺中删除IRS1和IRS2时,消除了胰岛素/ IGF-1信号传导,并且强烈抑制了肺肿瘤。
“在这个肺癌模型中,几乎所有的动物通常都会在KRAS激活后的15周内死亡,”Kalaany说,他同时也是哈佛医学院的助理教授和麻省理工学院和哈佛大学布罗德研究所的副成员。“但是Irs1和Irs2缺失的患者则完全正常——我们在10到15周时几乎没有看到肿瘤。”
阻断肿瘤的治疗方法
Kalaany和她的同事对这一结果感到兴奋,因为IGF-1抑制剂药物已经可以像Irs1/2缺失一样有效地阻断胰岛素/IGF-1信号。但他们也知道那个肿瘤细胞经常想出变通办法。
“我们决定让动物活得更长时间,并肯定在16周大约16周,我们开始看到一些肿瘤,”卡拉尼说。“那么我们问道,这些肿瘤细胞如何克服IRS1和IRS2的丧失?”
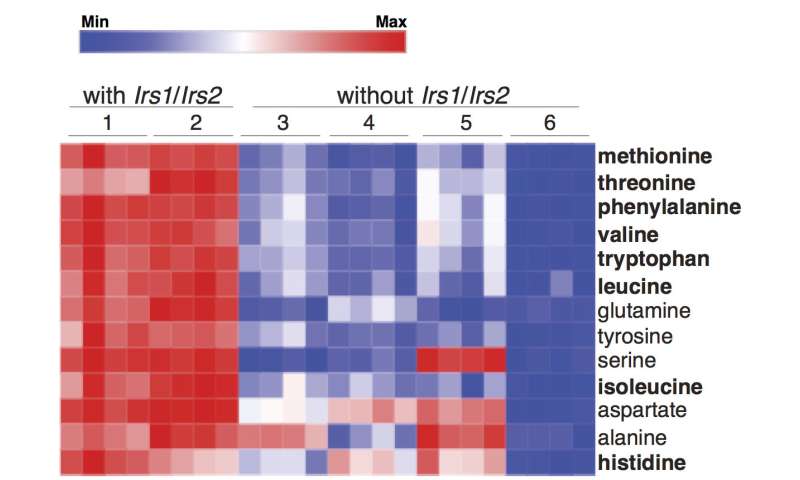
代谢图谱显示,缺乏Irs1/2的肿瘤细胞的必需氨基酸水平显著降低,而必需氨基酸是蛋白质的组成部分。然而,在细胞外,氨基酸是丰富的。研究人员发现,当它们抑制时也会发生同样的情况胰岛素/ IGF-1在人肺肿瘤中的信号传导。
“像IGF-1这样的生长因子告诉细胞营养物质就在周围,所以当你抑制它们的信号传递时,肿瘤细胞就不会吸收氨基酸并认为它们饿了,”Kalaany解释说。“但是我们发现肿瘤细胞可以对此进行补偿,并分解自己的蛋白质来产生氨基酸。"
癌症的代谢方法
事实证明,现有药物也可以抑制蛋白质的分解,比如抑制自噬(字面意思是“自我吞噬”)的氯喹,它正在一些癌症药物试验中使用,以及硼替佐米(Velcade),一种被称为蛋白酶体抑制剂的药物,用于治疗多发性骨髓瘤。
当Kalaany的团队给人注射肿瘤细胞缺少Irs1/2的小鼠,肿瘤就不能生长。当他们添加蛋白质分解抑制剂时,生长几乎完全被抑制。
Kalaany说,尽管这两种药物以及IGF-1抑制剂耐受性都很好,但在使用任何联合疗法时都需要小心,以避免产生毒性。她补充说,如果针对肺部,这种疗法也可能更安全。
就像最近的另一个研究在Kalaany的胰腺癌实验室中,目前的研究表明靶向癌细胞的代谢是一种有效的武器。
“我们的工作试图识别肿瘤中的代谢依赖性和漏洞,”卡拉尼说。“如果我们确定合作者,我们会喜欢进行临床试验非小细胞肺癌将IGF-1抑制剂与自噬抑制剂或蛋白酶体抑制剂组合。“
进一步探索












用户评论