鉴定了支持膳食应激下血细胞产生的分子
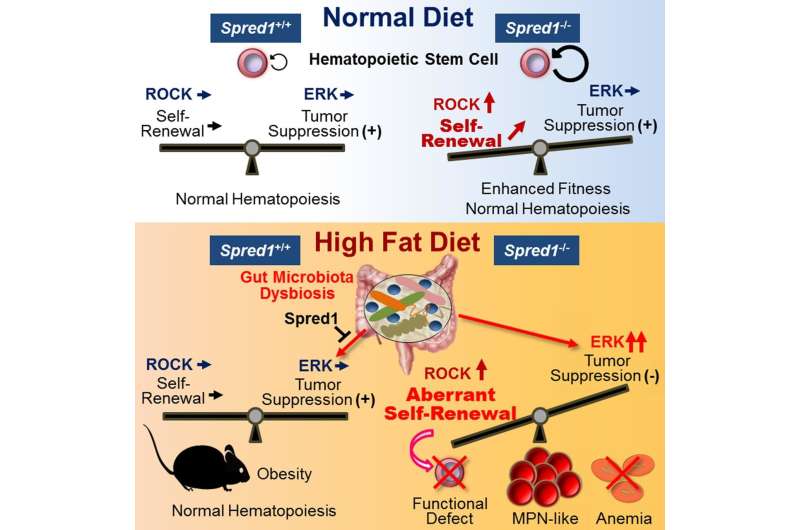
卡泽瓦大学的研究人员报告细胞干细胞SPRED1分子如何参与造血干细胞自我更新。用小鼠模型的实验表明,在正常情况下,Spred1充当负调节器,而在饮食诱导的压力下,它可以保护造血稳态。
通过所谓的造血干细胞(HSC)来调节血细胞的产生,其存在于骨髓中。众所周知,在某些应激条件下,例如老化或炎症,HSC的自我更新能力 - 茎的关键特性细胞- 分泌。现在,由Yuko Tadokoro和Atsushi Hirao来自Kanazawa大学的一支研究人员研究了由HSC的稳态(平衡自我更新)中称为Spred1的分子发挥作用。他们的主要发现是,Spred1保障HSC宿舍在小鼠受到高脂饮食的情况下。
研究人员之所以研究Spred1蛋白,是因为它与c-Kit结合,c-Kit是一种参与调控星状细胞发育和调控的信号传导过程的分子。对spred1缺陷小鼠的实验表明,在没有压力的情况下,该蛋白对正常的造血(血液细胞成分的形成)不是至关重要的。Spred1的缺失促进了HSC的自我更新,延长了细胞寿命,增强了竞争力,增强了对HSC的抵抗力生理压力。
Tadokoro和Hirao还使用Spred1缺乏的小鼠作为Legius综合征的模型,这是一种由Spred1基因突变引起的病理状态。他们发现,缺乏Spred1不会导致白血病的发生,因此得出结论,这种蛋白质不是传统的肿瘤抑制因子。
在野生型小鼠中,衰老,移植和用脂多糖治疗(模拟细菌感染的程序)上调的SPRED1蛋白。科学家认为,这种上调可能导致生理压力条件下的HSC功能障碍。
然而,当研究人员观察高脂肪饮食对spred1缺陷小鼠的影响时,他们发现饮食触发了一种特殊类型的血癌的发展。这一发现清楚地表明,Spred1确实在调节造血稳态中发挥了重要作用。
Tadokoro和Hirao的研究强调了Spred1和造血之间的复杂关系,并建立了蛋白质功能和饮食应激之间的联系。关于未来的研究,科学家们得出结论:“研究饮食因素在干细胞自我更新中的病理生理作用,探索spred1介导的HSC自我更新控制方法,可能会发现预防饮食相关疾病和恶性肿瘤的创新技术。”
进一步探索













用户评论