新型药物治疗部分恢复了小鼠的听力
小分子药物是第一个在遗传性人耳聋的癌症形式的小鼠模型中保持听证,报告爱荷华大学,爱荷华州,爱荷华州,奥卡瓦城,国家聋人聋人研究所和其他沟通障碍研究所(nidcd)。这项研究,它出现在线细胞该研究揭示了一种耳聋的分子机制(DFNA27),并提出了一种新的治疗策略。
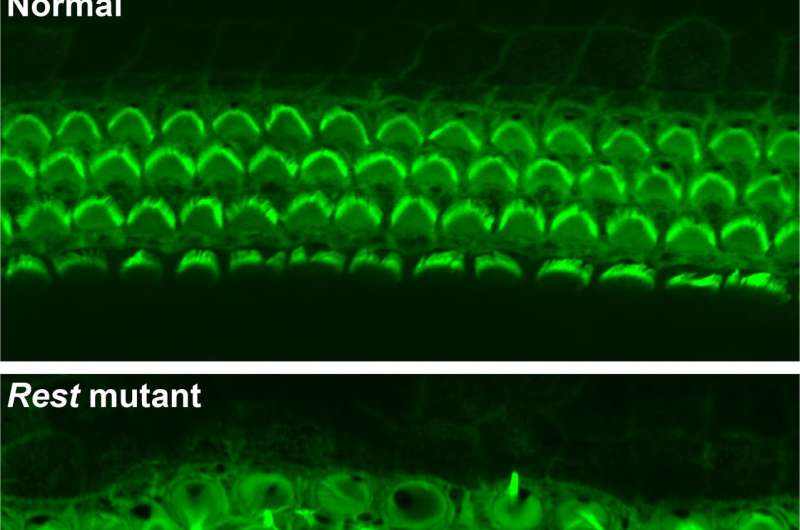
“我们能够部分恢复听力,特别是在较低的频率,并保存一些感官毛细胞Thomas B. Friedman博士说,他是NIDCD人类分子遗传学实验室的主任,也是这项研究的合著者。“如果更多的研究表明小分子药物对治疗DFNA27有效的话耳聋对于人类来说,使用类似的方法可能对其他遗传性的渐进性听力损失也有效。”
这项进展的种子是在十年前播下的,当时由Friedman和Robert J. Morell博士领导的NIDCD研究人员分析了一个被称为LMG2的大家庭成员的基因组。在LMG2家族中,耳聋是一种显性遗传,这意味着孩子只需要从父母那里遗传一个有缺陷的基因副本就可以拥有耳聋进步的听力损失。
研究人员将导致耳聋的突变定位在第4号染色体上一个叫做DFNA27的区域,该区域包含了大约12个基因。然而,NIDCD研究小组无法确定突变的确切位置。
后来,爱荷华大学的研究人员对小鼠RE1沉默转录因子(Rest)基因进行了研究,这为解释DFNA27形式的渐发性耳聋提供了重要线索。Botond Banfi医学博士和Yoko Nakano博士,是目前这项研究的主要作者,他们发现老鼠的休息是通过一种不寻常的感官机制来调节的细胞这种调节对老鼠的听力至关重要。由于与小鼠Rest基因对应的人类基因位于DFNA27区域,爱荷华州和NIDCD的研究人员合作重新研究了DFNA27进行性耳聋的奥秘。
蛋白质的编码序列是通过将基因的外显子片段拼接在一起,同时编辑其间的片段而产生的。由此产生的分子作为特定蛋白质的模板。以前的大多数研究都忽略了这一点外显子因为在大多数细胞中,这个小的外显子没有被编辑到Rest mRNA中。REST蛋白质的正常功能是关闭只需要在极少数细胞类型中活跃的基因。
当Banfi的团队删除老鼠的Rest基因的第4外显子时,老鼠的内耳毛细胞死亡,老鼠变得失聪。许多本应活跃的基因在毛细胞死亡前就被关闭了。通过合作,Friedman和Banfi的团队确定了LMG2家族中的失聪突变。他们发现,该突变位于第4外显子附近,改变了第4外显子的边界,并干扰了毛细胞中REST的失活。
“我们发现,将第4外显子合并到REST信使rna中就像一个进入开关感觉毛孔。它关闭了休息,允许打开许多基因,“Banfi说。”其中一些开启了基因对毛细胞存活和听力都很重要。”
研究人员使用Banfi的外显子4缺陷小鼠作为DFNA27耳聋的模型。由于REST通过一个称为组蛋白去乙酰化的过程来抑制基因表达,他们想看看阻断这个过程是否能减少听力损失。通过使用抑制这一过程的小分子药物,研究人员能够关闭REST并部分恢复听力。
NIDCD的科学主任安德鲁·格里菲斯(Andrew J. Griffith)说:“这些结果显示了研究遗传性耳聋的分子机制的价值。”“通过跟踪这些基因线索,我们发现了新的和意想不到的途径,在这种情况下,可以发现人类意想不到的潜在治疗策略。”
进一步探索







用户评论