发现和维持慢性炎症性肠病的免疫细胞

在临床前实验中,伯明翰阿拉巴马大学的劳里哈灵顿,博士和同事发现了一种产生和维持慢性炎症性肠病的免疫细胞的子集。这些细胞可能成为改善或治愈克罗恩病和溃疡性结肠炎的潜在治疗靶标。
此外,如果这个CD4 T的子集细胞在其他自身免疫疾病中起着类似的作用,例如1型糖尿病或类风湿性关节炎,它们也可以是治疗的目标。
“我们认为这些细胞可能处于一些自动炎症性疾病中,”UAB科技部,发展和综合生物学部的副教授Harrington说。“我们的希望是,如果我们可以治疗这些细胞,它可能是治疗。”
炎症肠道疾病或者IBD,有两种形式:克罗恩病,可以影响胃肠道的任何部分,但大多数往往发生在较低的小肠中;和溃疡性结肠炎,发现在大肠和直肠中。在这两种情况下,延长的炎症损害了GI道,伴随着包括持续腹泻和腹痛的症状。
IBD是一种由功能失调免疫应答引起的自身免疫性疾病,但是如何解决方法免疫细胞引起慢性炎症和病理学是未知的。在IBD中,细胞因子干扰素-γ通过一种称为CD4 T细胞的免疫细胞大量产生,但有关干扰素-γ在疾病中的作用存在矛盾的信息。
哺乳动物中的免疫系统通过各种不同免疫细胞的大规模相互作用而起作用。目标是触发将识别和消除感染细菌或病毒的反应,然后在感染消失时关闭该响应。与此同时,免疫应答不应该攻击一个人自己的细胞,一个称为自身免疫的有害攻击。
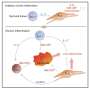
这种紧密控制的免疫从骨髓中的血液干细胞开始,其具有区分大量不同的免疫细胞。干细胞本身可以无限期地分裂。干细胞产生称为的中间体细胞祖细胞。祖细胞可以分开一段时间,但不是无限期地分开,并且它们具有进一步分化成一种或几种类型的完全分化的免疫细胞的能力。
作为一个例子,效应CD4 T细胞是可以分化为在IBD中发现的各种类型的T辅助细胞的祖细胞。
在结肠炎的小鼠模型中,第一作者Boyoung Shin及其同事发现,效应CD4 T细胞存在于分化状态的光谱中,细胞的致病潜力与分化状态直接相关。
它们能够将CD4 T细胞分为两组:产生不产生干扰素-γ的干扰素-γ的CD4 T细胞和CD4 T细胞。当转移到健康小鼠时,干扰素-γ阳性CD4 T细胞不能赋予结肠炎,并且这些细胞不需要维持疾病。
相反,它是致病性的干扰素-γ-阴性CD4 T细胞。这些细胞能够引发和维持肠道炎症。该组展示了干细胞样转录签名,其支持自我更新的能力和抵抗编程的细胞死亡,称为细胞凋亡。它们还在发炎的肠道中连续地播种过终点分化的干扰素 - γ-产生细胞。
研究人员还鉴定了干扰素-γ-阴性CD4 T细胞中的糖基转移酶酶,其呈正常调节茎的转录因子。
与哈灵顿研究类似,一群不同的研究人员最近发现存在持续控制慢性病毒感染的CD8 T细胞的不同子集,并且这种独特的细胞群是由其干燥品质的特征。
除了哈灵顿和胫骨,研究的共同作者,“疗效CD4 T细胞与祖母潜力介导慢性肠炎,”发表在实验医学杂志,是罗伯特L.克拉克斯特和苏珊L. Bellis,Uab系,发育和综合生物学系;和Philip A. Kramer和Victor M. Darley-Usmar,UAB病理系。
进一步探索













用户评论