候选药物可能对更广泛类别的脑癌有效
一项路德维希癌症研究解释了为什么被诊断为脑癌多形性胶质母细胞瘤(GBM)的患者中,表皮生长因子受体(EGFR)(一种细胞表面蛋白)的一种特殊突变会导致更具侵袭性的肿瘤和较差的总体生存率。
这也表明,这种致命形式的GBM可能对路德维希公司开发的抗体药物敏感,该药物目前正在临床试验中,用于治疗GBM不同亚型肿瘤。GBM是成人大脑中最常见也是最致命的一种癌症。
“这是患者数据指导分子分析的完美典范,”研究联合领导者Frank Furnari说,他是Ludwig癌症研究所的圣地亚哥分支机构成员。该研究,也由宾夕法尼亚大学(omenn)Zev Binder和Donald O'Rourke领导,出现在7月9日期刊中癌症细胞。
肿瘤学家早就知道,至少一半的GBM肿瘤中存在EGFR改变。Binder领导的一个团队最近发现了EGFR中丙氨酸289 (A289)位点的“错义”突变,导致了一种更具侵略性和更致命的癌症亚型。(错义突变会导致基因编码的蛋白质中一个氨基酸被另一个氨基酸取代。)这种突变的患者在诊断后平均存活时间仅为6个月,而其他EGFR患者存活时间为14 - 17个月突变。
路德维希的研究人员与瑞典斯德哥尔摩大学(Stockholm University)的生物物理学家和结构生物学家劳拉·奥雷拉纳(Laura Orellana)合作,她曾假设EGFR等突变A289可以响应MAB806,由Ludwig研究人员开发的单克隆抗体,用于靶向EGFRVIII突变。(EGFRVIII是具有胶质母细胞瘤的受体的众所周知的突变体。)由于药物公司ABVIE的药物被“武装”,目前在美国的III期临床试验中。
在Furnari实验室的PERTDOC之间的Binder和Amy Haseley Thorne会议上会议开始了两组之间的合作,这将测试Orellana的假设的治疗潜力。
利用他们在分子分析方面的专业知识,路德维希团队精确地指出了EGFR的作用A289突变可导致恶性肿瘤增多,胶质母细胞瘤患者整体生存率较差。Furnari说:“我们使用小鼠模型表明,这种突变的机制是通过蛋白酶MMP1的表达增加侵袭。”
MMP1是基质金属蛋白酶-1的简称,由细胞分泌,分解细胞外基质。细胞外基质是由蛋白质和分子组成的复杂网络,帮助组织中的细胞相互结合,并帮助细胞通信。
当细胞需要重新排列自己的时期,例如胚胎发育和细胞分裂时,通常在时段中表达MMP1。但Ludwig团队表明了脑部肿瘤与EGFR的小鼠A289V.突变也表达了MMP1,使其更具侵入性,导致较差的存活率。
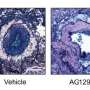
Ludwig和Upenn集团证实,作为Orellana的假设,患有EGFR的小鼠中的肿瘤A289mAb806突变也易感。当有EGFR的老鼠A289V.用MAB806治疗突变,它们的脑肿瘤缩小并使动物寿命明显更长。
Furnari说,作为这项研究的后续研究,他的团队正在调查EGFR是否存在A289也可能存在于其他癌症类型中。“如果是这样,”Furnari说:“它建议我们的Ludwig抗体也将对这些癌症有一些效用。”








用户评论