脂肪生产和燃烧在肥胖的小鼠的肝脏中同步

发表在《科学》杂志上的一项新研究表明,喂食高脂肪食物的老鼠会形成新的肝脏昼夜节律,影响脂肪积累和燃烧的方式细胞由宾夕法尼亚大学佩尔尔曼医学院的研究人员。该团队发现,随着肝脏脂肪的产量增加,令人惊讶的是,身体燃烧脂肪的能力也是如此。这些相反的生理过程每天达到5点左右达到峰值活动,说明过早,昼夜节律和肝脏脂肪积聚之间的意外连接。
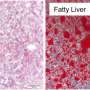
“我们知道,肥胖会导致脂肪在肝脏中堆积,从而导致炎症甚至肝炎,肝衰竭, 乃至肝癌资深作者Mitchell Lazar博士说,他是宾夕法尼亚大学糖尿病、肥胖和代谢研究所主任,内分泌学、糖尿病和代谢科主任。“这正迅速成为一个巨大的问题,因为这些条件会导致需求的增加肝移植更糟糕的是,可以致命。“
虽然全世界的10亿人受到营养不良的不利影响,但有剩余的百亿人体验过多的卡路里摄入量,或“过度营造”,这导致肥胖等代谢紊乱包括2型糖尿病、心血管疾病、脂肪肝、高血压和癌症。拉扎尔说:“研究营养过剩的有害影响是当务之急,特别是在代谢紊乱已经达到流行程度的美国。”
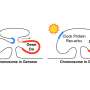
这昼夜节律脂肪的创造和燃烧遵循是每24小时内发生的生理过程。在分子水平,这些循环涉及在几乎每种细胞中表达的核心钟蛋白的反馈回路。该内部计时器的作用是以组织特异性方式整合环境刺激和遗传信息以控制节奏基因表达。
这一时间表的失调越来越被认为是代谢紊乱的一个危险因素。例如,夜班工人和有睡眠障碍的人患代谢性疾病的风险更高。了解影响昼夜节律和代谢紊乱之间关系的机制对于制定治疗肥胖相关疾病的有意义的治疗策略是必要的。
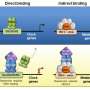
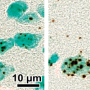
“我们推测,饮食诱导的这些反对肝脏脂肪代谢过程的同步是对营养过剩环境的一种反应,导致脂肪燃烧超过速度。脂肪堆积第一作者、拉扎尔实验室博士后关东寅博士说。
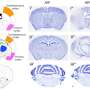
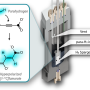
这种生理学的24小时时钟方面会通知计时疗法的做法,这涉及在最抗冲和耐受性的时候涉及给药,以提高效果和减少毒性。该团队发现了节奏的燃烧脂肪由称为PPAR-α的蛋白质控制,这是称为匹配的药物的靶标,这些药物已经用于降低血液中的脂质。肝脏中PPAR-α的量也达到5点左右。
从这种协调来看,拉扎尔的团队询问是否会在PPAR-Alpha处于最高水平时在一天的特定时间施用短暂的PPAR-α药物。研究人员观察到,当在下午给予时,肝脏脂肪减少了肝脏脂肪,而不是在早上给出的时候。
类似于他汀类药物(胆固醇降低药物)在睡前服用,“我们的结果支持,由于PPAR-α的节奏,降低肝脏和血脂水平的药物在一天的特异性时期可能更有效,“拉扎尔说。“这种原则更接近治疗肝脏代谢疾病可能确实有益于患者,因为最近的研究表明,PPAR-α表达在人体中振荡肝”。
进一步探索








用户评论