FDA召回心脏用药Valsartan,引用癌症问题
美国食品和药物管理局发布了含有活性成分缬沙坦的几种药物的自愿召回,该药物用于治疗高血压和心力衰竭。
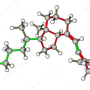
“该召回是由于杂质,N-硝基二甲胺(NDMA)在召回的产品中发现,FDA在陈述中表示。”然而,并非所有含有Valsartan的产品都被召回。“
官员称,NDMA被归类为可能的人类致癌物质 - 一种可能导致癌症的物质。他们表示,寻找调查结果是基于最近的实验室测试的结果。
FDA表示,致癌物质的存在是“认为与制造活性物质的方式变化有关。”
“我们仔细评估了在美国销售的缬沙坦的药物,我们发现,这些特定公司出售的瓦萨兰不符合我们的安全标准。这就是为什么我们要求这些公司立即采取行动保护患者,“FDA药物评估和研究中心杰特伍德科克博士说。
FDA说,已经服用召回药物的患者应该立即联系药剂师或医生。
要确定是否已召回特定产品,患者应查看药品名称和公司名称在他们的处方瓶的标签上。如果信息不在瓶子上,耐心应联系药房,分配药物。
召回的特定药物是:
- 缬沙坦,主要药品。
- 瓦斯坦坦,索尔科医疗保健。
- 瓦斯坦坦,Teva Pharmaceuticals Industries Ltd.
- 缬沙坦/氢氯噻嗪(HCTZ),索尔科医疗保健。
- 缬沙坦/氢氯噻嗪(HCTZ),Teva Pharmaceuticals Industries Ltd.
©2018 Miami Harald
分发由Tribune Content Agency,LLC。
引文:FDA召回心脏用药缬沙坦,引用癌症问题(2018年,7月17日)从Https://medicalXpress.com/news/2018-07-fda-recalls-heart-medication-valsartan.html检索癌症问题
本文件受版权保护。除了私人学习或研究目的的任何公平交易外,没有书面许可,没有任何部分。内容仅供参考。










用户评论