宿主抗体通过改变细菌基因表达来塑造肠道微生物群
日本综合医学科学riken中心的研究人员发现了如何在肠道中分泌的抗体促进有益细菌的生长。他们的学习,将于7月24日出版实验医学杂志,显示免疫球蛋白A(IgA)抗体可以改变细菌基因的表达,允许不同的细菌种类彼此配合并形成可以保护身体免受疾病的群体。
据估计,每天在成人肠中产生两到五克IgA。Iga是针对有害的第一行防线,致病细菌在胃肠道中,它还能促进健康的微生物群的生长——“好”的社区细菌那个居住在肠道里。平均成人在其肠道中有于千种细菌,可改善肠和免疫系统的功能,显着影响人类健康和疾病。
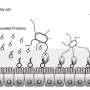
LED由Keiichiro Suzuki,第一作者Akira Nakajima及其同事在京都大学和Riken Yokohama Institute探讨了IgA如何促进健康肠道细菌的生长。抗体通常争取有害细菌通过识别细菌表面的特定蛋白质。但是Suzuki和他的同事们发现,即使是能够识别非细菌蛋白质的IgAs也能覆盖在健康肠道细菌的表面,因为附着在IgAs尾部的糖分子可以与脂多糖分子结合,而脂多糖分子存在于许多不同种类的细菌上。
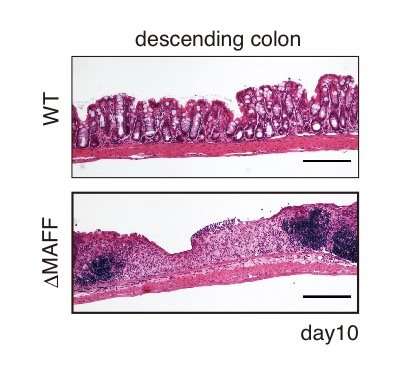
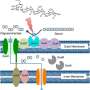
突出的人体肠道细菌伯曲面Thetaiotaomicron.(B.θ.)对IgA涂层特别敏感。Suzuki和他的同事们发现,暴露在IgA中会导致过敏反应B.θ.这两种蛋白质在结构上与许多其他菌株共享,研究人员将这些分子命名为黏液相关功能因子(MAFFs)。这些蛋白质似乎有帮助B.θ.在肠道的粘膜中生长,并产生允许其他的代谢物有益的细菌,如梭太物,茁壮成长。用一个菌株接种的小鼠B.θ.不能上调MAFFs的肠道微生物群发生改变,更容易发生肠道炎症或结肠炎。
“我们知道免疫球蛋白A以某种方式贡献了肠系健康,但发现这种新机制 - 制造制度 - 实际上促进了栖息于肠道粘膜膜的细菌之间的共生,”苏祖博士说。“Maff System也存在于人类中,”他继续,“这是一个有趣的研究目标,但仍有很大的调查目标。我们需要识别其分子目标并找出其表达式如何调节邻近的遗传元素,希望回答这些问题可能导致开发新方法的疗法或预防炎症性肠病。"
进一步探索











用户评论