新方法增加了大脑类器官缺失的功能
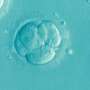
在凯斯西储大学医学院、纽约干细胞基金会(NYSCF)研究所和乔治华盛顿大学的一项合作研究中,研究人员开发了一种新的方法,可以从人类干细胞中生成微型3d版本的大脑,称为“类器官”。通过为细胞提供一个环境,让它们像在实际人脑中那样相互作用,大脑类器官使研究人员能够观察大脑发育,研究疾病,并测试有前景的新药。这项新技术今天在网上发表自然方法他创造了第一个有髓鞘形成能力的类器官,比以往任何时候都更接近地模拟了大脑的结构和功能。
NYSCF致力于加速神经系统疾病的治疗,并开发更好的方法供社区使用干细胞疾病研究是实现这一目标的关键部分,”NYSCF首席执行官苏珊·l·所罗门说。“这种新方法源于NYSCF社区的长期合作,我们为这种合作关系所带来的工作感到非常自豪。”
这项研究是由纽约scf - robertson干细胞研究员校友Paul Tesar博士,凯斯西储大学医学院Donald博士和Ruth Weber Goodman创新疗法教授以及遗传学和基因组科学副教授领导的。NYSCF研究所的这项工作由NYSCF高级首席研究员Valentina Fossati博士领导,他与Tesar博士合作多年,解开了多发性硬化症等疾病的秘密。他们的合作始于2011年NYSCF年度创新者撤退(NYSCF在研究界建立桥梁的众多努力之一)上的一次对话。
所罗门指出:“当Tesar博士和Fossati博士第一次在NYSCF创新者静修会上见面时,科学的火花立即开始迸发。”“正如这项研究所表明的那样,这种类型的合作对于加速研究和治疗至关重要。”
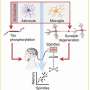
大脑类器官技术通过概括不同脑细胞类型的组织,彻底改变了该领域,但之前的类器官缺少一个关键成分:少突胶质细胞。少突胶质细胞是产生髓磷脂的脑细胞,髓磷脂是一种包裹在神经纤维上并帮助神经元发送信号的物质。当髓鞘受损时,细胞不能有效地相互交流,导致麻木、反应丧失、运动不协调和疼痛等症状。在髓磷脂缺失的情况下,如多发性硬化症或脊髓损伤,少突胶质细胞被认为发挥着重要的作用,但人们对其知之甚少。将具有髓鞘化能力的少突胶质细胞纳入类器官模型提供了一种新的方法来研究这一过程在这些疾病中如何出错,并测试修复它的方法。
基于NYSCF研究所最初开发的从干细胞中生成少突胶质细胞的方案,凯斯西储大学的研究小组确定了一种特定的生长因子组合,可以生成包括少突胶质细胞的类器官。他们证明了髓磷脂增强药物增加了类器官中少突胶质细胞的髓鞘形成,这表明这些类器官可能在药物的临床前试验中有用,以修复有缺陷的髓鞘形成。研究人员还使用这种方法从Pelizaeus-Merzbacher病(一种罕见但致命的遗传髓鞘形成障碍)患者的干细胞中生成类器官瀑样成功地模拟了疾病的特征。NYSCF的研究人员使用不同的干细胞系独立复制了该方案,这对证明可重复性至关重要。
“我们的新方法让我们更清楚地了解大脑是如何细胞在多发性硬化症或pelizae- merzbacher等疾病中起作用并相互作用,它为开发恢复髓鞘形成的新疗法提供了很大的希望,”Tesar博士解释道。“我期待着继续与NYSCF研究所合作,更好地理解和治疗髓鞘形成障碍。”
特萨尔博士和福萨蒂博士的团队将把这种新的类器官方案应用于未来的多发性硬化症研究,以测试针对少突胶质细胞刺激髓鞘形成的药物的有效性。这项工作的一部分将在未来三年内得到纽约州干细胞科学(NYSTEM)的资助。Tesar博士还获得了2017年NYSCF-Robertson干细胞奖,以表彰他在神经系统疾病干细胞研究方面的开创性工作。他的NYSCF资助是支持当前研究的几个奖项之一。
Fossati博士说:“我们非常感谢与Tesar博士的富有成效的合作,并为能够为这一重要技术提供验证而感到兴奋,以确保它可以被社区采用。”“通过填补大脑类器官模型的关键空白,我们相信这个新方案将提升对大脑器官模型的研究多发性硬化症以及各种复杂的神经系统疾病,包括阿尔茨海默病和帕金森病。”
进一步探索