研究人员在老鼠。反向先天性失明
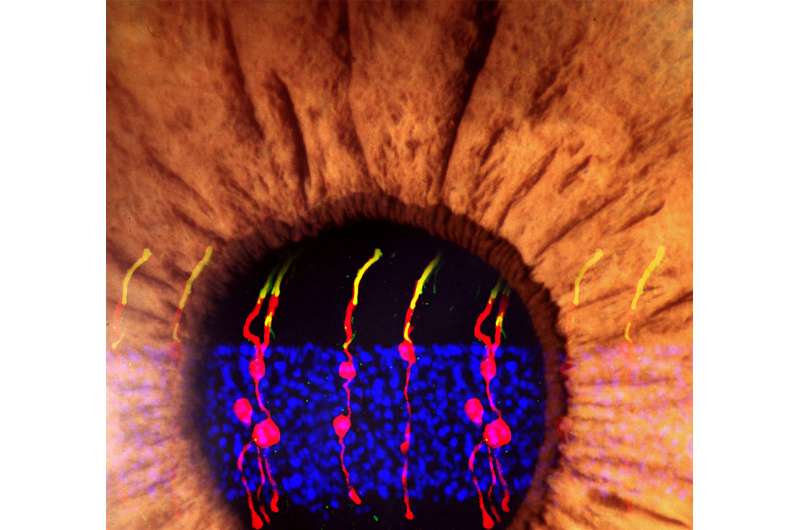
研究由美国国家眼科研究所(NEI)逆转了小鼠先天性失明改变支持细胞在视网膜上称为穆勒神经胶质杆光感受器。结果提前努力再生治疗致盲的疾病,如年龄相关性黄斑变性和色素性视网膜炎。一份报告的结果今天在网上出现自然。NEI是美国国立卫生研究院的一部分。
“这是第一次报告的科学家重新编程穆勒成为功能性神经胶质杆光感受器在哺乳动物视网膜托马斯表示:“联合国Greenwell博士NEI项目主任视网膜神经科学。“低光棒让我们看到,但它们也可以帮助保护锥体光感受器,这对颜色视觉和高视力很重要。锥往往死在后期眼疾。如果棒可以从眼内再生,这可能是治疗疾病的策略影响光感受器的眼睛的。”
感光细胞是视网膜感光细胞的眼睛时,大脑信号激活。在哺乳动物,包括老鼠和人类,感光细胞不能再生。像大多数神经元,一旦成熟他们不分裂。
科学家们长期研究的再生潜力穆勒神经胶质因为在其他物种,比如斑马鱼,把伤害和可以转化为视网膜光感受器和其他神经元。后的斑马鱼可以恢复视力严重视网膜损伤。然而,在实验室里,科学家可以诱导哺乳动物穆勒神经胶质的行为更像他们做的鱼。但它需要组织受伤。
“从实用的角度来看,如果你想视网膜再生恢复一个人的视野,是适得其反伤害它首先激活穆勒神经胶质,“陈老板说,博士,副教授眼科和眼部干细胞项目主任伊坎在西奈山医学院,纽约。
“我们想知道如果我们能计划穆勒神经胶质成为杆感光细胞在活的老鼠没有伤害它的视网膜,”陈先生说,这项研究的首席研究员。
在第一阶段两级的重编程过程的团队推动穆勒在正常小鼠神经胶质除以注入他们的眼睛和一个基因一种叫做β-连环蛋白的蛋白质。几周后,他们给老鼠的眼睛注射因素鼓励新分裂细胞发展成杆光感受器。
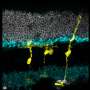
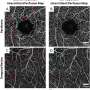
研究人员使用显微视觉跟踪新形成的细胞。他们发现新成立的杆光感受器看起来结构没有不同于真正的光感受器。此外,突触结构,使棒与其他类型的视网膜神经元内也形成了。确定穆勒glia-derived杆光感受器功能,他们检测了小鼠的治疗先天性失明,这意味着他们出生没有功能杆光感受器。
在对待老鼠天生失明,穆勒glia-derived棒一样有效地开发他们在正常小鼠。功能上,他们证实,新成立的棒与其他类型的视网膜神经元突触。此外,光反应记录视网膜神经节cells-neurons携带信号光感受器的大脑,而测量大脑活动确认新棒实际上是视觉通路中的集成电路,从视网膜到大脑的初级视觉皮层。
陈的实验室正在进行行为研究确定小鼠是否具有恢复能力执行视觉任务,比如水迷宫任务。陈还计划技术是否适用于人类视网膜组织培养。
进一步探索











用户评论