团队界定了在ewing sarcoma中关键遗传异常的行动机制
马萨诸塞州综合医院(MGH)研究团队已经使用了外观蛋白酶编辑工具来调查如何在儿童和年轻成年人中促使育种肉瘤的遗传异常 - 第二个最常见的骨癌 - 释放肿瘤生长。在他们的论文中在期刊上基因与发育研究人员表明,阻断融合蛋白EWS-FLI1在基因组中的结合和激活的特异性“增强剂”位点可防止促进肿瘤生长的基因的表达。
“我们以前表明EWS-FLI1与GGAA微卫星的结合在基因组中重复,将这些位点转化为活性增强剂,”Mguel Rivera,MD,MG,MG,癌症研究中心,癌症研究中心,报告的联合高级提交人。“现在我们使用了新的简胶组编辑工具来关闭单独的微卫星,并证明它们在控制附近的表达方面具有重要的功能基因这对此至关重要瘤生长。”
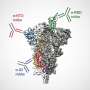
EWING SARCOMA是由称为染色体易位的遗传改变引起的,其中染色体22基因EWS与染色体11基因FLI1融合,导致融合蛋白EWS-FLI1的产生。2014年癌细胞由Rivera和Bradley Bernstein,MD,博士学位领导的研究,也发现了MGH病理学和癌症研究中心,发现EWS-FLI1有两个可能导致肿瘤生长的性质:常规转化微卫星重复的DNA元素在基因组中发现活性增强剂,刺激其他基因的表达和对调节基因转录的其他因素的表达和抑制。从本质上讲,EWS-FLI1均在气体上进行阶梯,并将制动器脱落给肿瘤生长。
目前的研究旨在直接测试之间的链接微卫星EWS-FLI1激活,癌症相关基因的表达和肿瘤生长。研究人员专注于GGAA微卫星的重复核苷酸鸟嘌呤和腺嘌呤 - 通常是无活性的,但在ewing肉瘤中被EWS-FLI1结合并激活。
调查人员使用了一种基于新的CRISPR的系统,将阻遏模块带到邻近GGAA微卫星的位点,其在肌肉瘤细胞中,这显着降低了刺激肿瘤生长的附近基因的表达。相反,在未表达融合蛋白的癌细胞中对GGAA重复的抑制对基因表达没有影响。最后,沉默于已知调节的特定重复表达Sox2,一种作为癌基因的转录因子导致小鼠母羊肉瘤肿瘤的大小的显着降低。
“发现在肿瘤中特异性的基因组中的增强剂等调节区域,但不在正常细胞中可能指出新的治疗机会,”哈佛医学院病理学助理教授Rivera说。“我们现在正致力于识别重要的肿瘤特异性增强剂肿瘤生长在ewing sarcoma和其他类型的癌症。“
进一步探索










用户评论