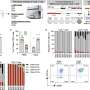
研究将BAP1蛋白与肾脏,眼睛,胆管和间皮瘤癌症的肿瘤抑制联系起来
德克萨斯大学医学硕士安德森癌症中心的研究人员已通过调节一种称为肥大的细胞死亡形式,表明与BRCA相关蛋白1(BAP1)如何用作肾脏,眼睛,胆管,间皮瘤和其他癌症的肿瘤抑制基因扩大潜在的治疗研究领域。这项研究的结果是由Boyi Gan,Ph.D.,实验放射肿瘤学副教授的副教授,于9月10日在线发行的自然细胞生物学。
甘说:“尽管BAP1经常在多种癌症中突变或删除,但抑制肿瘤的过程尚不清楚。”“我们的研究实现了BAP1调节的靶基因和相关生物学过程的全面鉴定癌细胞,并确定了将铁铁作用联系到的BAP1介导的表观遗传机制肿瘤抑制。”
铁凋亡是最近确定的调节形式细胞死亡由胱氨酸的消耗(一种对癌细胞生长和存活至关重要的氨基酸的耗竭),以及通过脂质上称为活性氧(ROS)的分子载体过量生产,与脂质有关,与癌症有关,是与癌症有关的,并且是某些疗法的靶标。
Gan说:“螺栓吞噬在结构,遗传和生化上与其他形式的受调节细胞死亡(如骨动作)不同。”“众所周知,细胞死亡,最著名的细胞凋亡在肿瘤抑制中起着重要作用。然而,铁凋亡在肿瘤生物学中的作用和调节机制仍然很大程度上尚未开发。”
GAN的团队描述了BAP1如何编码与其他酶和细胞成分相互作用以调节基因的关键酶,从而导致肿瘤通过铁凋亡抑制。研究人员发现,用ROS诱导剂的治疗导致BAP1癌细胞中与其他类似癌症的壮铁相关细胞死亡的大幅度更多细胞不表达BAP1。他们还发现,BAP1通过介导抑制称为SLC7A11的胱氨酸“转运蛋白”来促进铁铁作用。
Gan说:“我们表明BAP1通过SLC7A11和铁凋亡抑制了肿瘤的发育,并且与癌症相关的BAP1突变体失去了抑制SLC7A11并促进铁铁作用的能力。”“总之,我们的结果发现了先前未批准的机制将铁铁杀伤耦合到瘤抑制。”
进一步探索