新的帕金森氏症转基因模型阐明了疾病生物学
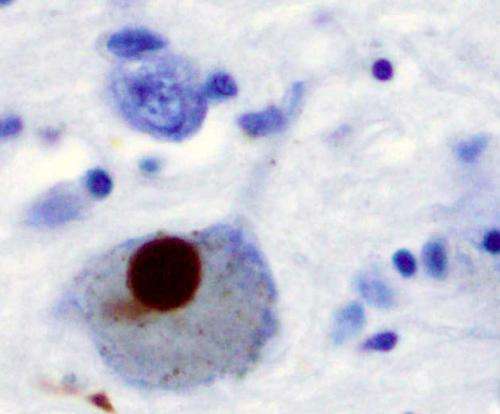
帕金森病(PD)是一种神经退行性疾病,临床表现为运动异常和休息时震颤。在大脑中,PD的标志是蛋白质α-突触核蛋白(αS)的积累,形成被称为路易体的团块,损害神经健康。既往研究表明,异常αS可改变细胞膜功能,导致细胞死亡。来自布里格姆妇女医院的研究人员开发了一种独特的小鼠模型,可以诱导pd样αS聚集,导致静息性震颤和异常运动控制。该小鼠模型对左旋多巴有反应,与PD患者类似。该研究小组使用这种转基因小鼠模型的结果发表在本周的杂志上神经元.
“很难找到针对αS聚集的有效治疗方法,”主要作者Silke Nuber博士说,他是BWH安·罗姆尼神经疾病中心的讲师。“因此,有必要开发反映长期变化的小鼠模型,包括αS的路易样聚集和相关的紧密PD表型,以更好地理解导致PD启动的机制。”
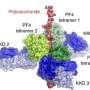
在一个健康的大脑中,该实验室首次报告(Bartels等,自然αS可以以螺旋折叠四聚体的形式正常出现(αS的四个单位相互缠绕),这种形式可以抵抗异常αS单体的聚集。为了给帕金森病的大脑建模,Nuber和她的团队创造了一种新的转基因小鼠,它具有降低四聚体的突变,导致αS沉积,多巴胺损失和神经毒性。
“通过这些新的小鼠,我们开始检查四聚体降低突变的上游作用及其与PD的相关性,”Nuber说。“我们的假设是,上游正常四聚体对过量单体的不稳定会导致PD的变化。”
为了检验四聚体消除突变对αS病理的影响,研究团队创建了多个具有特定αS突变的小鼠系,这些突变会长期减少四聚体,增加自由单体,并导致神经元功能障碍和变性。然后,他们将新的四聚体消除小鼠与表达正常人类αS蛋白的小鼠和只具有单一家族性PD αS突变的小鼠进行比较。仔细并排评估与PD相关的关键生化、组织和行为特征。
新的四聚体切除小鼠显示出关键的pd样变化,包括年龄依赖性αS聚集在改变的神经元和独特的异常运动。这些变化均源于抑制正常αS四聚体的形成。这些发现有力地表明,大脑中αS的正常状态需要四聚体。作者得出结论,四聚体向单体的转移很可能引发PD。他们还注意到,这种表现型在雄性小鼠中更为突出,这让人联想到PD,他们计划在BWH的女性大脑倡议框架内继续研究这一发现。
“我们现在可以从一个全新的角度来审视PD。我们可以考虑稳定生理αS四聚体,这是一个全新的治疗概念,作为预防或延迟PD发病的一种手段。”
“根据我们实验室在解释阿尔茨海默病早期阶段的经验,我们在一段时间前决定将类似的方法应用于PD中发生的不同蛋白质异常,”医学博士丹尼斯·塞尔科(Dennis Selkoe)说,他是这篇论文的资深作者,也是BWH安·罗姆尼神经疾病中心的联合主任。“我们认为这是独一无二的小鼠模型表明我们在2011年发现的αS的四聚体形式对正常的神经元功能是必要的,因此取消四聚体有直接的pd样结果。这PD鼠标模型将为全新的治疗方法提供一条新途径。”