Discovery为减缓或逆转MS提供了新的机会
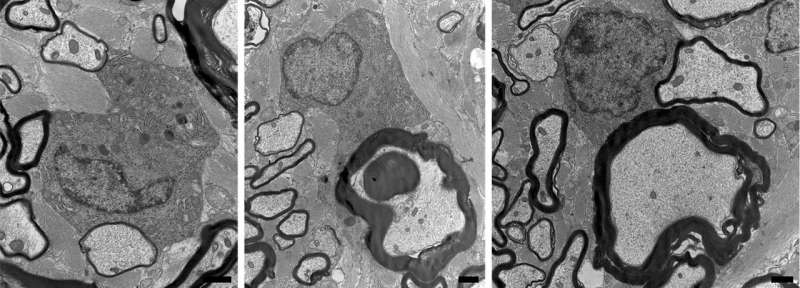
失去绝缘体的神经细胞不能再携带重要信息,导致多发性硬化症常见的麻木、虚弱和视力问题。一项新的研究表明,一种被忽视的来源可能能够取代失去的绝缘,并提供一种治疗多发性硬化症等疾病的新方法。
一种叫做神经元的细胞使中枢神经系统工作,它通过一种叫做轴突.当轴突被包裹在一种叫做髓鞘.
威斯康星大学麦迪逊兽医学院的神经科学家伊恩·邓肯说:“当你失去髓磷脂时,轴突不能以正常速度传导,或者根本不传导。”“如果有足够多的神经细胞受到影响,比如多发性硬化症患者的脱髓鞘大面积受损,就会出现与神经系统相关的临床症状。”
髓磷脂是由少突胶质细胞这些细胞可以接触到附近的几个轴突,将部分轴突包裹在保护膜中髓鞘.
人们一致认为,一旦轴突失去了髓磷脂,唯一的办法就是从新鲜的少突胶质细胞开始。只有少突胶质细胞起源于前体称为少突细胞祖细胞可以在轴突上涂上一层新的髓磷脂,这是一种教条。因此,针对脱髓鞘的MS治疗聚焦于在脱髓鞘区域(称为斑块)招募祖细胞,并刺激它们生长。
然而,由邓肯领导的研究人员在今天发表在《美国国家科学院院刊从祖细胞开始并不是重组的唯一途径。在经历了髓磷脂严重缺失的猫和猕猴身上,邓肯发现已经充分发育的少突胶质细胞正在伸展,并开始再次用髓磷脂包裹受影响的轴突。
如果真有问题的话,那就是成年少突胶质细胞要想帮助修复受损的轴突,可能仍然需要与其他轴突上存活的髓鞘部分(称为“节间”)保持连接。
邓肯说:“如果这个细胞仍然具有生物活性,并维持着这些节间,它就可以将过程重新延伸到这些脱髓鞘的节段。”他的工作得到了美国国家多发性硬化症协会的支持。“这些过程可以产生新的髓鞘,最终比以前的节间更薄、更短。”
但正如邓肯及其同事在2009年报告的那样,即使更薄的髓磷脂也能恢复神经功能。
喂了几个月辐照食物的猫会在整个神经系统中出现严重的髓磷脂损失。当猫恢复正常饮食时,由于髓磷脂得到广泛修复,神经功能得到了恢复。
作为这种疾病的实验室模型,猫的脱髓鞘问题是不寻常的。
邓肯说:“研究脱髓鞘和再髓鞘脱髓鞘的实际模型是在喂食一种叫做铜蛋白酶的毒素的老鼠身上。”“但这种毒素会杀死少突胶质细胞。所以,在研究老鼠时,你自然不会看到任何原始的少突胶质细胞开始重组。”
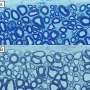
在这项新研究中,研究人员观察了猫的神经组织,发现了一种独特的髓磷脂马赛克——被厚层髓磷脂包围的轴突(在轴突自身生长时形成)与其他被薄层髓磷脂包围的轴突穿插在一起。
邓肯说:“对这种马赛克外观最有可能的解释是幸存的寡头。”“在髓鞘脱臼后不会出现厚的髓鞘,只有薄的髓鞘。存活下来的成人少突胶质细胞靠近这些脱髓鞘部位,使它们可能成为髓鞘修复的候选者。”
果不其然,研究人员发现少突胶质细胞与猫脊髓中的厚髓鞘和薄髓鞘都有连接。
当他们回到几十年前的脱髓鞘猴子模型时,他们也发现了这种关联。20世纪70年代,凯斯西储大学的神经科学家Dimitri Agamanolis试图制作另一种人类脱髓鞘疾病的模型——由维生素B12缺乏引起的亚急性联合退行性变。阿伽马诺利斯保存了猴子神经组织的样本块,并与邓肯分享。猴子的髓鞘损伤与猫的髓鞘损伤相似。
邓肯说:“你也可以在猴子身上看到,单个少突胶质细胞连接到成熟的髓鞘,而成熟的髓鞘也有延伸到脱髓鞘轴突的过程。”
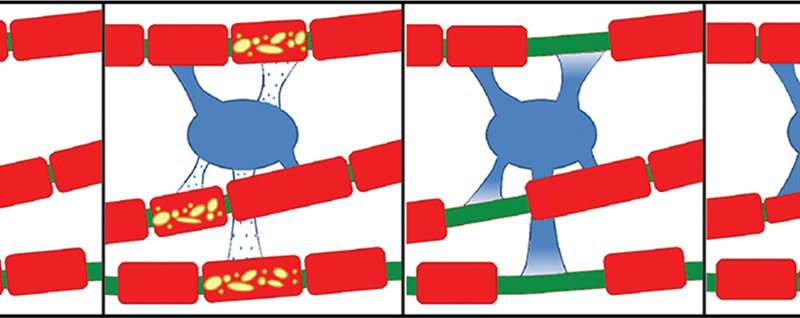
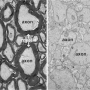
威斯康辛大学麦迪逊分校的研究人员招募了Grahame Kidd和克利夫兰的私人研究实验室Renovo Neural,重建了一堆猫的电子显微镜图像神经细胞三维图像显示,少突胶质细胞在脊髓上和下延伸,维持着成熟的髓磷脂,并使受损的鞘重新形成鞘。
邓肯说,这一过程在人类多发性硬化症患者身上的进展可能还不够快,不足以帮助减缓疾病的进展。或者过多的少突胶质细胞可能会失去太多的节间连接,导致它们失去活性或死亡。
但成熟的髓磷脂产生细胞的修复能力的发现,为减缓或逆转疾病提供了新的机会。
邓肯说:“目前的重点是促进寡聚祖细胞的数量和它们的分化,特别是向成年少突胶质细胞分化。”“这项工作提供了一个不同的目标。”
这一目标需要新的治疗方法——例如,寻找药物,使少突胶质细胞向受损的髓鞘伸出新的生命线。
邓肯说:“在对抗复杂疾病时,比如多发性硬化症,你手头的工具越多越好。”“如果这些成年人细胞在某种程度上是可以招募的,我们应该想办法做到这一点。”
进一步探索












用户评论