内聚下调促进造血干细胞老化
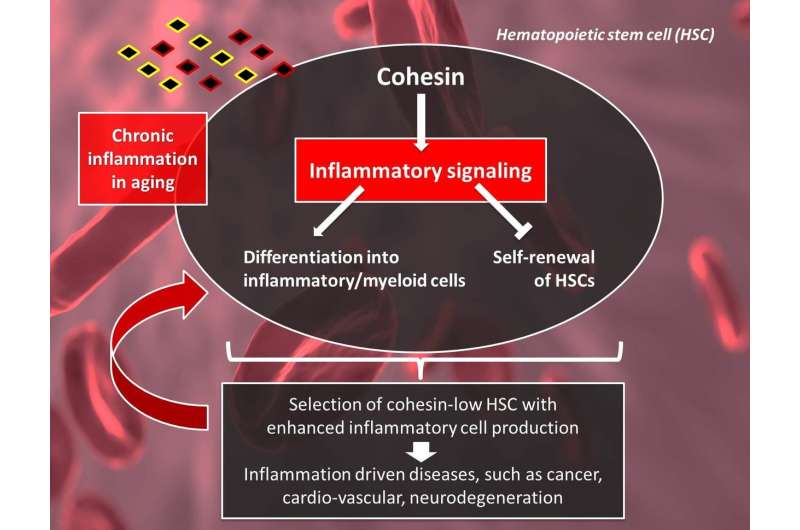
衰老的特征是炎症增加和干细胞功能下降。这些过程之间的关系仍然没有被完全理解。德国耶拿莱布尼茨衰老研究所(FLI)的研究人员发现了蛋白内聚蛋白在造血干细胞(HSCs)中介导炎症信号的新作用。正常分化过程中需要内聚蛋白进行基因调控,但衰老过程中的慢性炎症通过不断激活内聚蛋白介导的炎症信号,损害了造血干细胞的功能和自我更新。造血干细胞内聚减少,自我更新增加和倾斜分化被选择,类似于造血老化的标志。
耶拿。随着人体衰老,炎症增加,这加速了与衰老相关的疾病的发展,这个过程被称为“炎症化”。这一过程也会影响造血系统,炎症会指示系统中的干细胞(造血干细胞(如造血干细胞)表现出异常的自我更新和分化为炎症/髓系细胞的不平衡,这反过来又导致进一步的炎症反应加速。干细胞老化的驱动因素仍然不完全清楚。通过对这一过程的机制了解,有望开发出改善衰老过程中健康状况的疗法。
德国耶拿莱布尼茨衰老研究所-弗里茨利普曼研究所(FLI)的研究人员现在发现,内聚复合物——一个DNA夹钳——在HSC对炎症的反应中起着重要作用,因此似乎推动了造血老化和炎症反应的关键特征。研究结果现发表在实验医学杂志。
造血系统在老化和炎症
一个良好工作的造血系统是基于造血干细胞分化成血液系统中所有重要细胞类型并作为干细胞进行自我更新(自我更新)的平衡潜能。在衰老和增长的过程中,慢性炎症,造血系统的平衡丢失了。HCSS显示重新流量受损,偏差分化:这意味着它们更有可能分化为炎症/骨髓细胞而不是淋巴细胞。
转录因子NF-κB控制许多炎症相关基因。该途径在许多情况下被激活炎性疾病。在衰老过程中,已发现hsc中NF-κB信号通路增加。然而,增强的NF-kB信号通路对造血干细胞衰老的功能影响尚不清楚。
内聚蛋白是NF-κB信号转导的关键调节因子
耶拿莱布尼茨衰老研究所(FLI)的研究人员及其合作者研究了衰老和炎症过程及其对造血系统的影响。“我们知道衰老伴随着炎症的增加,但慢性炎症对造血干细胞和生物体衰老的后果还不完全了解,”陈志阳博士,博士后研究人员他解释了这项研究背后的动机。
目前的研究增加了我们的理解,并表明内聚介导了造血干细胞中的炎症信号,这在衰老和炎症过程中具有功能性后果。内聚蛋白对造血干细胞的正常分化很重要,但在衰老和炎症过程中,相同的调节环限制了干细胞的功能,特别是造血干细胞的自我更新能力。衰老的造血干细胞不能下调内聚介导的炎症信号,这些信号在衰老过程中长期被激活。
FLI的高级组长K. Lenhard Rudolph教授总结说:“这种持续炎症的机制耗尽了干细胞池,并推动干细胞向炎症细胞错误分化。”反过来,这些损伤增加了对低表达的异常干细胞的选择cohesin这显示出自我更新和分化为炎性/髓系细胞的异常增加——这是造血的一个特征系统,加速机体老化。”干预衰老造血干细胞中慢性炎症的分子环路细胞是否有助于减缓衰老和癌症、心血管和神经退行性疾病等与衰老相关的疾病的发展炎症。
进一步探索














用户评论