医学科学家描述了肝癌的最佳免疫治疗策略
Kaist医学科学家介绍了一种涉及T免疫细胞疲惫的新途径,提供了用于设计癌症患者免疫检查点梗死最佳策略的证据和理由。
它们成功地将肝细胞癌组区分离出肝脏渗透的肿瘤渗透免疫细胞组成癌症患者。与Asan Medical Centre合作进行的贵族免疫治疗学研究证实了对肝脏的适用性癌症患者,为定制医学提供新的路径以及翻译研究的新模式。
当癌症发生时,身体会激活T细胞以去除癌细胞。肿瘤构成抑制T细胞功能的环境。此时,渗透T细胞作为PD-1蛋白递送至细胞表面。它的活动减少,然后耗尽。
免疫系统能够破坏癌细胞,但有时,癌细胞可以适应和突变,有效地隐藏免疫系统。一种发展的机制之一,以防止破坏免疫系统是在功能上沉默效应器T细胞,称为T细胞耗尽,该方法主要由免疫检查点分子如PD-1,TIM-3和LAG-3介导。
最近的突破和促进免疫检查点抑制剂(ICIS)等抗PD-1的临床结果单克隆抗体(mAb)和抗CTLA-4 mAbs通过免疫激活对癌症进行巨大潜力。免疫检查点抑制剂在几种类型的癌症中表现出显着的临床益处,导致他们在临床实践中的广泛应用。
抗PD1阻断抗体是这类药物中最代表性的药剂之一。然而,了解癌症中T细胞疲惫的生物学和临床意义一直挑战。一位凯师研究团队由苏敏公园教授领导现在举报了肝细胞癌(HCC)中T细胞耗尽的异质性及其潜在的临床意义胃肠病学12月4日。
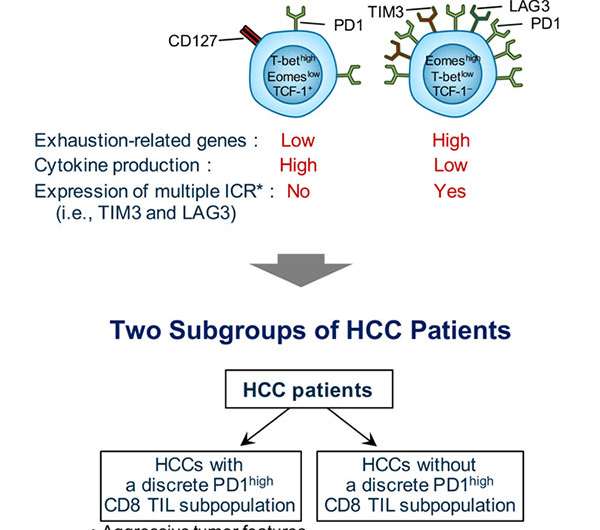
该团队揭示了通过HCC中CD8 + T细胞中的差异PD-1表达水平确定的异质T细胞耗尽状态。作者发现,与HCC患者的高PD-1表达(PD-1High CD8 + TIL)的肿瘤浸润的CD8 + T细胞功能效果损害,与具有低的人相比,递送其他免疫检查点受体,如TIM-3和/或LAG3PD-1表达(PD-1LOW CD8 + TILS)。
此外,基于这些结果,作者根据PD-1High CD8 + Tils的存在或不存在定义了两种不同的HCC患者亚组。他们发现,HCC患者PD-1High CD8 + TILs与更积极的生物肿瘤特征和生物标志物相关,预测其对抗PD1治疗的反应。此外,研究小组表明,只有PD-1高CD8 +直至患有肿瘤浸润的CD8 + T的HCC患者细胞表达多种免疫检查点受体,其可以通过组合免疫检查点梗死的组合进一步重新生物。
Park教授说:“本研究发现的HCC患者的新分类可以用作生物标志物,以预测目前癌症免疫疗法的反应(抗PD-1治疗)。”他还表示,他们将继续对各种类型的癌症中的T细胞疲惫和活化进行研究,这可能导致更好地了解对癌症的T细胞反应,从而为未来的癌症免疫疗法提供证据,以实现延长的最终目标癌症患者的存活。
进一步探索














用户评论